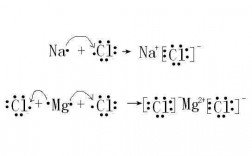本篇目录:
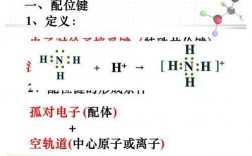
离子键的形成
离子键的形成是通过两个或多个原子或化学集团失去或获得电子而成为离子后形成。原子轨道的重叠与电子转移 离子键的形成首先起源于原子轨道的重叠。当两个原子相互靠近时,它们的原子轨道会开始相互重叠。
阴、阳离子通过静电作用形成离子键,所以活泼的金属单质(如 $K、Na、Ca、Mg$ 等)与活泼的非金属单质(如 $FClBrOS$ 等)化合时,一般形成离子键。

离子键是化合物中阴阳离子的相互作用。离子键是原子团或原子间的作用力,形成是是离子化合物,存在与金属阳离子(或铵根离子)和非金属阴离子(或原子团)之间。离子键存在于离子化合物中,其他的都是共价键。
mgo离子键形成过程?
1、MgO是由镁离子(Mg2+)和氧离子(O2-)通过离子键形成的离子化合物。
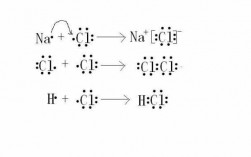
2、离子键是由电子转移(失去电子者为阳离子,获得电子者为阴离子)形成的。即正离子和负离子之间由于静电引力所形成的化学键。
3、离子键的形成首先起源于原子轨道的重叠。当两个原子相互靠近时,它们的原子轨道会开始相互重叠。这会导致电子从一个原子的原子轨道转移到另一个原子的原子轨道,这个过程称为电子转移。这个电子转移过程是形成离子键的关键步骤。

4、氟化镁MgCl2的形成过程为:形成氯化镁时,镁原子失去电子,形成二价镁离子,氯原子得到电子,形成一价氯离子,镁离子和氯离子通过离子键形成氯化镁。
5、形成正负离子,由静电作用形成的。共价键的成因较为复杂,路易斯理论认为,共价键是通过原子间共用一对或多对电子形成的,其他的解释还有价键理论,价层电子互斥理论,分子轨道理论和杂化轨道理论等。
形成离子键的过程必定是氧化还原反应
1、可以,因为一定会生成一种化合物,而化合物只有两种类型所以一定是其中一种,所以一定有离子键或共价键生成。
2、根据元素的氧化/还原性强弱,即易得/失电子的程度。判断化学键两端的两个原子的电负性(下表)相差越大,极性越强(相差足够大的时候就变成离子键了)。键的极性是由于成键原子的电负性不同而引起的。

3、离子键的形成首先起源于原子轨道的重叠。当两个原子相互靠近时,它们的原子轨道会开始相互重叠。这会导致电子从一个原子的原子轨道转移到另一个原子的原子轨道,这个过程称为电子转移。这个电子转移过程是形成离子键的关键步骤。
4、原子通过得失电子形成离子,注意是得失,不是和别的原子共用。
5、任何离子键的形成过程必定有电子的得与失,否则就不能由中性原子或者原子团形成带电离子。你的那个nah的问题,非常有趣。
到此,以上就是小编对于离子键形成过程动画的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏