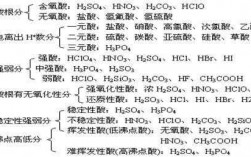
本篇目录:
探究稀盐酸的氢氧化钠溶液是否能发生化学反应,设计了三套方案
能使酚酞变红。NaCl溶液、水显中性,HCl溶液显酸性,不能使酚酞变红。实验现象:加了酚酞的NaOH溶液为红色,滴加HCl溶液后,溶液逐渐变浅,至恰好反应,溶液变成无色。
实验原理:酚酞遇碱性变红色。(OH- + 2H+ =H2O)实验现象:原红色的氢氧化钠溶液,加入稀盐酸后,变成无色。

所以,氢氧化钠和碳酸钠混合后跟稀盐酸反应,由于氢氧化钠的碱性比碳酸钠的碱性要强得多,盐酸先跟氢氧化钠反应。所以一开始是不会有现象的。
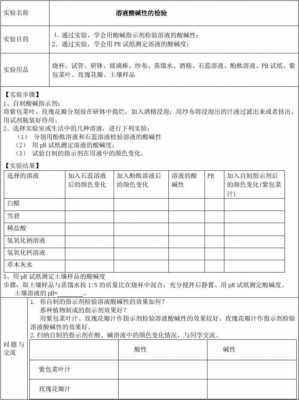
实验内容 实验现象 结论 【实验1】取一支试管加入少量氢氧化钠溶液,再逐滴滴入稀盐酸观察现象。
...氧化钠溶液与稀盐酸反应后的溶液。请设计实验探究氢氧化钠与盐酸是否...
1、能使酚酞变红。NaCl溶液、水显中性,HCl溶液显酸性,不能使酚酞变红。实验现象:加了酚酞的NaOH溶液为红色,滴加HCl溶液后,溶液逐渐变浅,至恰好反应,溶液变成无色。
2、实验步骤:在试管中加入适量的氢氧化钠溶液,滴几滴酚酞 用胶头滴管在试管中滴加稀盐酸 实验现象:试管中的溶液由红色变成无色 结论:当试管中溶液变成无色时,氢氧化钠和盐酸正好反应。
3、实验原理:酚酞遇碱性变红色。(OH- + 2H+ =H2O)实验现象:原红色的氢氧化钠溶液,加入稀盐酸后,变成无色。
人教版九年级下册化学《溶液的形成》教案
[交流结果]在蔗糖溶液中,溶质是蔗糖,溶剂是水;在氯化钠溶液中,溶质是氯化钠,溶剂是水。
溶液 实验9-1 溶液的形成 演示,观察现象。如何从微观上理解这一现象?蔗糖表面的分子在水分子的作用下,向水里运动扩散,并均一地分散到水分子中去了。
溶液的概念:一种或几种物质分散到另一种物质里形成的均一的、稳定的混合物,叫做溶液 溶质:被溶解的物质。可以是一种或几种,可以是固、液、气三态 溶剂:能溶解其它物质的物质。只能是一种。
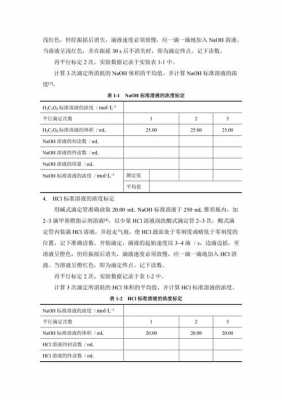
溶质分散到溶剂中形成溶液的过程,叫做物质的溶解。
到此,以上就是小编对于溶液实验报告的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏