本篇目录:
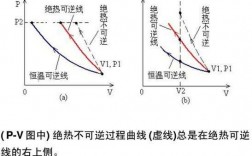
绝热膨胀
1、绝热膨胀是指气体在膨胀过程中不与外界交换热量,即系统内部的热量不流入或流出。在绝热条件下,气体的压力、体积和温度之间的关系可以通过绝热过程的定律来描述,如泊松定律或理想气体状态方程。
2、绝热膨胀是指与外界没有热量交换,但气体对外界做功,气体膨胀。根据热力学第一定律,可证明这是等熵过程,在这个过程中气体体积增大,压强降低,因而温度降低。所以绝热膨胀经常用于降低气体的温度,起到冷冻的效应。
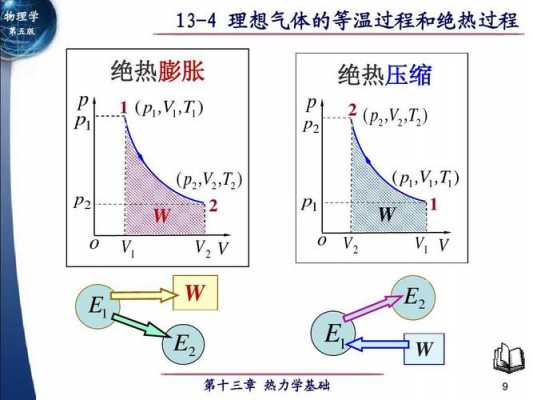
3、热膨胀是指与外界没有热量交换,但气体对外界做功,气体膨胀。根据热力学第一定律,可证明这是等熵过程,在这个过程中气体体积增大,压强降低,因而温度降低。所以绝热膨胀经常用于降低气体的温度,起到冷冻的效应。
4、体积增加,温度就会降低。绝热膨胀:膨胀过程中与外界绝热,那么,压力会降低,或者温度降低,或者压力和温度都降低。绝热膨胀和等压膨胀的过程是等压膨胀:压力不变,体积增大。绝热膨胀:膨胀过程中与外界绝热。
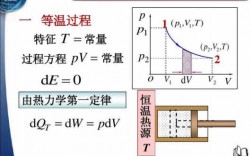
5、绝热膨胀与等温膨胀有什么区别 在等温过程中,最大限度的热量被转移到了外界,使得系统温度恒定如常。绝热过程中,热量没有逃逸,因而温度有上升(下降)。
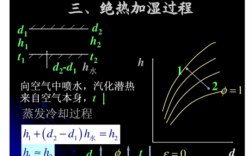
6、但是空气是热的不良导体,在这一瞬间可以近似认为微元体没有与周围环境进行热量交换(绝热),因此是一个绝热膨胀过程。这个过程空气的温度迅速降低,进而在短时间内引起凝结,形成降雨。
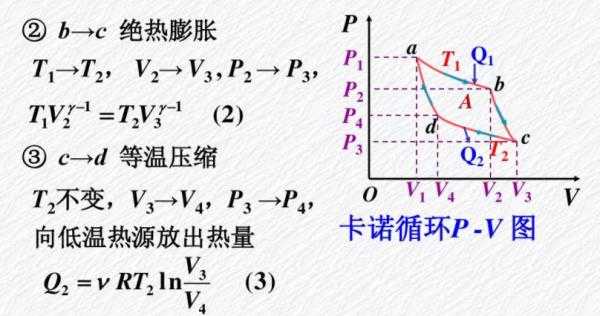
理想气体的热膨胀过程可以分为哪两种方式
1、绝热过程。自由膨胀过程 由于体系经历绝热过程,故与外界无热交换。又由于气体向真空自由膨胀,外压为零,故体系对环境做功也为零。
2、理想气体的真空自由膨胀的过程是一种不可逆的热力学过程,理想气体过程中气体在一个绝热的系统内膨胀,外界和系统之间没有功和热的交换。真实气体在自由膨胀时会有温度的变化。
3、(2) 理想气体绝热自由膨胀过程是非准静态过程,除初,末态外,系统每一时刻都处于非平衡态。
绝热膨胀温度变化
绝热膨胀温度会降低。分析:因为绝热自由膨胀后,δQ=0,δW=0,dU=0。由于是范德华气体,膨胀后气体体积增加导致气体分子间势能增大,而dU=0,所以气体平均动能必然降低,温度下降。

温度会降低,因为绝热自由膨胀后,δQ=0,δW=0,dU=0.由于是范德华气体,膨胀后气体体积增加导致气体分子间势能增大,而dU=0,所以气体平均动能必然降低,温度下降。
当一个物体系统没接受热而进行状态变化时,体积一旦出现变化,就会发生温度变化,这种变化称为绝热温度变化。如一个空气块移动到气压较低的环镜(与四周空气没有热量交换),会引起气块的体积膨胀,因而温度下降。
【答案】:绝热过程中,由于不吸收热量,系统对外作功是以自身内能减少为代价的,故内能减少,而理想气体的内能是温度的单值函数,所以系统的温度下降。
如何操作才能保证是绝热膨胀过程
1、(1) 在隔板迅速抽掉的瞬间,气体自由膨胀到整个容器,属于绝热膨胀过程。由于没有与外界有接触,因此没有传热发生,即传热为0。气体对外做功等于气体膨胀所对外界做的功,可以通过理想气体状态方程计算。
2、绝热过程的方程为:PdV+VdP=nRdT,dQ=dU+dW=0,dU=nCvdT。
3、规律:准静态绝热膨胀过程中理想气体的压强跟体积满足绝热方程:V=常数。
4、用良好绝热材料隔绝的系统中进行的过程,或由于过程进行得太快,来不及与外界有显著热量交换的过程,都可近似地看作绝热过程。
到此,以上就是小编对于绝热膨胀过程特点的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏