本篇目录:
- 1、理想气体绝热节流后,其状态参数熵,焓,温度各自怎么变化
- 2、理想气体绝热可逆膨胀的亥姆霍兹和吉布斯自由能为什么
- 3、气体反抗外压绝热压缩U等于多少
- 4、谁可以帮我比较通俗的解释一下熵、焓、等熵焓降这些专业名词?
理想气体绝热节流后,其状态参数熵,焓,温度各自怎么变化
压力降低 比容(单位质量的体积)增大 焓不变 内能不变 熵增大 如有不明欢迎追问。
对于理想气体,焓是温度的单值函数,所以绝热节流后焓值不变,温度也不变。对于实际气体,焓是温度和压力的函数,经过绝热节流后,温度降低、升高和不变3种情况都可能出现。

绝热又不对外界做功,根据稳定流动能量方程,可得节流前后Δh=0,即h1=h2。绝热节流前后工质的温度会发生变化,即节流的温度效应,温度可以升高、可以降低、也可以不变。但对于理想气体前后温度肯定是不变喽。
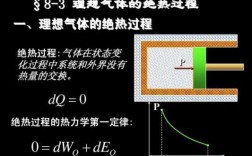
焓:热力学中表示物质系统能量的一个状态函数,常用符号H表示。数值上等于系统的内能U加上压强p和体积V的乘积,即H=U+pV。焓的变化是系统在等压可逆过程中所吸收的热量的度量。
理想气体绝热可逆膨胀的亥姆霍兹和吉布斯自由能为什么
1、楼上说错了,熵变是为零,但温度并不是变的,所以焓变不能确定,由△G=△H-△(TS)得,吉布斯函数变是不能确定的,同理,亥姆霍兹函数变也是不能确定的。
2、Gibbs自由能:dG《δWf(G表示Gibbs自由能) 其意义是:在等温、等压条件下,一个封闭的系统所能做的最大非膨胀共等于起Gibbs自由能的减少。
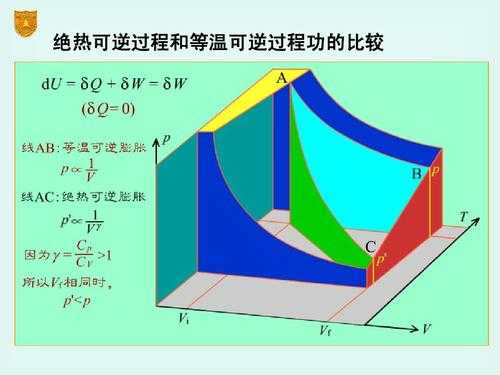
3、自由能指的是在某一个热力学过程中,系统减少的内能中可以转化为对外做功的部分。自由能(free energy)在物理化学中,按照亥姆霍兹的定容自由能F与吉布斯的定压自由能G的定义。吉布斯自由能是自由能的一种。
4、说明等温、等压、可逆过程中,体系对外所做的最大非膨胀功等于体系吉布斯自由能的减少值。若是不可逆过程,体系所做的功小于吉布斯自由能的减少值。
气体反抗外压绝热压缩U等于多少
1、对于理想气体,等温可逆过程,△U=△H=0,W=-nRTlnV2/V1,Q=-W。绝热可逆过程:Q=0,△U=W=-P外dV(恒外压)或△U=nCv,mdT,△H=nCp,mdT。可逆过程是指热力学系统在状态变化时经历的一种理想过程。
2、理想气体向真空膨胀,U=0、H=0、Q=0、W=0,S增加,一切都是因为T不变引起的。因为自由膨胀时间不计,来不及发生热交换,近似视作绝热,Q不变,而没有压力对气体做功,所以W为0,由热力学第一定律,T不变。

3、还有,有时候比如:2mol理想气体,T1=500k,P1=405Kpa。V1=0.0205M3,在P=206Kpa外压下绝热膨胀至平衡态T2=380k,P2=206KPa,V2=0.0312M。定容摩尔热容 Cv,m =3/2R。。计算功的时候,。
4、方程 对于理想气体,等温可逆过程△U=△H=0;W=-nRTlnV2/V1,Q=-W 绝热可逆过程:Q=0,△U=W=-P外dV(恒外压);或△U=nCv,mdT;△H=nCp,mdT。
谁可以帮我比较通俗的解释一下熵、焓、等熵焓降这些专业名词?
1、物理学家玻尔兹曼将熵定义为一种特殊状态的概率:原子聚集方式的数量。可精确表示为:S=K㏑W K是比例常数,现在称为玻尔兹曼常数。焓是一个热力学系统中的能量参数。焓是内能和体积的勒让德变换。它是SpN总合的热势能。
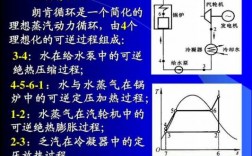
2、汽轮机以蒸汽为工质,熵反应蒸汽的品质,熵越低蒸汽品质越高;焓反应蒸汽蕴含的能量,焓越大蒸汽蕴含的能量越大 假如是个袋子,那么熵就代表着袋子的大小,焓就代表着袋子里装了多少东西。
3、焓可以在某种程度上表征工质做功能力。而熵微观上表征物质内部分子混乱程度。熵增分为熵流和熵产。熵流表示由于与系统与外界传热引起的熵增,熵产表示不可逆产生的熵增。熵和焓在工程上应用都极为广泛。
到此,以上就是小编对于绝热可逆焓变的计算的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏