本篇目录:
醋酸的电离方程式
1、醋酸的电离方程式为:CH 3 COOH=CH 3 COO - +H + 。醋酸一般指乙酸,乙酸的羧基氢原子能够部分电离变为氢离子(质子)而释放出来,导致羧酸的酸性。醋酸化学式CH3COOH,是一种有机一元酸,为食醋主要成分。
2、醋酸在水中的电离方程式为:CH3COOH CH3COO- + H+。醋酸在水中电离,形成醋酸根离子和氢离子。由于醋酸是弱电解质,所以不会发生完全电离。
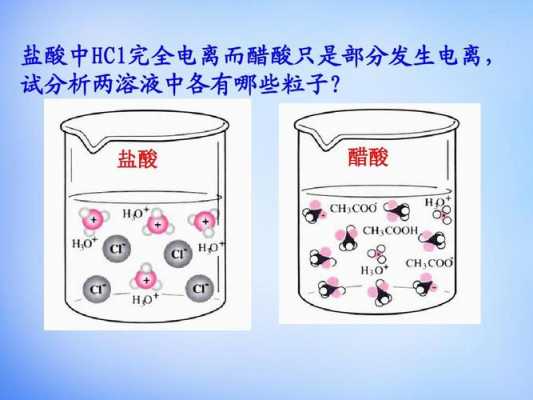
3、醋酸的电离方程式是:CH3COOHCH3COO-+H+ CH3COOH+OH-=CH3COO-+H2O 乙酸,也叫醋酸、冰醋酸,化学式CHCOOH,是一种有机一元酸,为食醋内酸味及刺激性气味的来源。
4、醋酸Ka=8×10^-5。Ka是弱酸的电离常数,条件是在室温下(25°C)。Ka表示弱酸的电离常数,Ka越大,酸性越强,pKa表示其负对数。
5、醋酸是一种弱酸,其在水中电离出的醋酸根离子(CH3COO-)可以发生水解反应,生成氢氧化物离子(OH-),从而表现出碱性。
6、加入醋酸铵,增大了溶液中醋酸根离子的浓度,会抑制醋酸的电离,使得氢离子浓度下降。电离平衡:具有极性共价键的弱电解质(例如部分弱酸、弱碱。
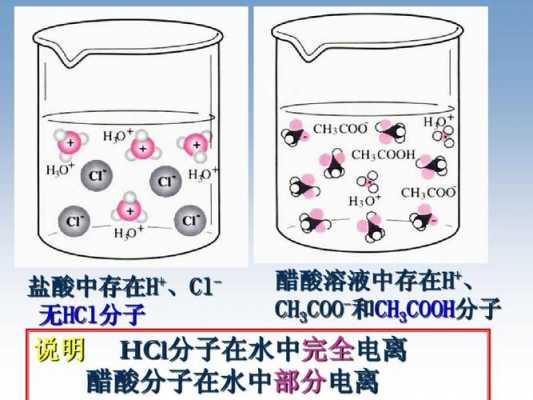
醋酸在水中的电离方程式
醋酸在水中的电离方程式为:CH3COOH CH3COO- + H+。醋酸在水中电离,形成醋酸根离子和氢离子。由于醋酸是弱电解质,所以不会发生完全电离。
醋酸在水溶液中的电离方程式:CH3COOH=CH3COO-+H+。醋酸的电离方程式为:CH3COOH=CH3COO-+H+。醋酸一般指乙酸,乙酸的羧基氢原子能够部分电离变为氢离子(质子)而释放出来,导致羧酸的酸性。
醋酸是一种弱酸,其在水中电离出的醋酸根离子(CH3COO-)可以发生水解反应,生成氢氧化物离子(OH-),从而表现出碱性。
醋酸的电离方程式是:CH3COOHCH3COO-+H+ CH3COOH+OH-=CH3COO-+H2O 乙酸,也叫醋酸、冰醋酸,化学式CHCOOH,是一种有机一元酸,为食醋内酸味及刺激性气味的来源。
醋酸在水中可以电离,但是是不完全电离,当有碱性物质存在的时候,就会促使弱酸电离,直至所有的分子全都以离子的形式存在。
碳酸氢钠(NaHCO3)和醋酸(CH3COOH)在水中反应会生成二氧化碳气体、水和乙酸钠(CH3COONa)。
醋酸的电离方程式如何书写?
1、醋酸在水中的电离方程式为:CH3COOH CH3COO- + H+。醋酸在水中电离,形成醋酸根离子和氢离子。由于醋酸是弱电解质,所以不会发生完全电离。
2、醋酸的电离方程式是:CH3COOHCH3COO-+H+ CH3COOH+OH-=CH3COO-+H2O 乙酸,也叫醋酸、冰醋酸,化学式CHCOOH,是一种有机一元酸,为食醋内酸味及刺激性气味的来源。
3、强电解质在水溶液中完全电离,在书写电离方程式时用符号“=”;在书写难溶性和微溶性强电解质的电离方程式时用符号“=”;有些电解质因条件不同,其电离方程式的书写形式也不同。
4、碳酸氢钠(NaHCO3)和醋酸(CH3COOH)在水中反应会生成二氧化碳气体、水和乙酸钠(CH3COONa)。
醋酸在水溶液中的电离方程式
对应的离子方程式:CH3COOH -- CH3COO- + H+ ,--改成可逆符号。
醋酸在水中的电离方程式为:CH3COOH CH3COO- + H+。醋酸在水中电离,形成醋酸根离子和氢离子。由于醋酸是弱电解质,所以不会发生完全电离。
醋酸的电离方程式是:CH3COOHCH3COO-+H+ CH3COOH+OH-=CH3COO-+H2O 乙酸,也叫醋酸、冰醋酸,化学式CHCOOH,是一种有机一元酸,为食醋内酸味及刺激性气味的来源。
在水中,醋酸根离子与水分子发生反应,生成醋酸和氢氧化物离子,从而使溶液呈现碱性。这是因为水解反应中生成的氢氧化物离子可以中和部分溶液中的氢离子,从而提高了溶液的pH值。
醋酸的羧基氢原子能够部分电离变为氢离子(质子)而释放出来,导致羧酸的酸性。
醋酸的电离平衡向哪移动?为什么?
也可以类比气体平衡,稀释相当于减压,平衡向粒子数较多的方向移动(类似于气体分子数较多),所以醋酸电离平衡正向移动。
根据平衡移动原理,稀释后,溶液中微粒总数(醋酸分子,醋酸根离子,H+的总和)减少,平衡将向着微粒数目增多方向移动,正方向是1个醋酸分子电离成2个离子的方向,既粒子增多的方向。
向右移动 因为加水使醋酸根和氢离子浓度减小,所以平衡向醋酸根和氢离子浓度增大的方向移动。
所以平衡向电离方向移动。也可以从离子运动的角度来理解:加水后,溶液中电离出的离子浓度降低,这些离子相遇的概率降低,也就是结合成电解质分子的概率降低,所以逆反应速率降低,平衡就向电离方向移动了。
加水后醋酸的物质的量会减小,醋酸根离子和氢离子的物质的量会增大,即平衡正移。加水后醋酸、醋酸根离子和氢离子浓度均会减小,因为加水稀释浓度减小,但醋酸浓度减小程度大,醋酸根离子和氢离子浓度减小程度小。
醋酸增加了,相当于反应物增加,化学平衡向右移动。同时溶液的醋酸浓度生高,选修4的课本讲过的,越稀越电离。越浓自然电离程度要降低。
醋酸的电离方程式是什么?
醋酸在水中的电离方程式为:CH3COOH CH3COO- + H+。醋酸在水中电离,形成醋酸根离子和氢离子。由于醋酸是弱电解质,所以不会发生完全电离。
醋酸的电离方程式是:CH3COOHCH3COO-+H+ CH3COOH+OH-=CH3COO-+H2O 乙酸,也叫醋酸、冰醋酸,化学式CHCOOH,是一种有机一元酸,为食醋内酸味及刺激性气味的来源。
醋酸Ka=8×10^-5。Ka是弱酸的电离常数,条件是在室温下(25°C)。Ka表示弱酸的电离常数,Ka越大,酸性越强,pKa表示其负对数。
到此,以上就是小编对于醋酸电离实验的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏