本篇目录:
对于理想气体的循环过程,其温度不变,内能不变,根据Q=cm△t,Q也不变...
1、问题出在能量守恒理解上,Q=CdT说明吸放热都用于内能变化,即用于温升,而没有顾及吸热还可用于做功。由于这里(等温)说明,吸收的热全部用于做功,从而内能不变。
2、Q:是热量。c:表示比热容。m:表示物体的质量。△t:表示物体的变化温度,即t-t0。该公式是计算物体吸收(放出)的热量。
3、正确。一定质量理想气体内能仅与温度有关。非理想气体具有分子势能,因此其内能与体积有关;若不给出物质状态,则其内能还与状态有关。如水沸腾时,温度不变,内能增加。
4、理想气体 ideal gas,有这么几个假设:A、气体的分子之间,除了碰撞的瞬间,其余时间里,没有任何相互作用。所以,就不存在分子势能的问题。内能就是所有分子的动能之和。也就是说,分子之间连万有引力都不存在。
水循环,碳循环和氧循环的过程中都伴随着能量的变化,对吗?
碳循环伴随能量流动。在生态系统内,能量流动与碳循环是紧密联系在一起的,碳循环本身就是物质循环中的一种,而在物质循环过程中能量流动,所以碳循环过程中伴随能量流动。
碳氧循环能体现自然界中的物质和能量转化。生物圈中的碳循环主要表现在绿色植物从大气中吸收二氧化碳,在水的参与下经光合作用转化为葡萄糖并释放出氧气,有机体再利用葡萄糖合成其他有机化合物。
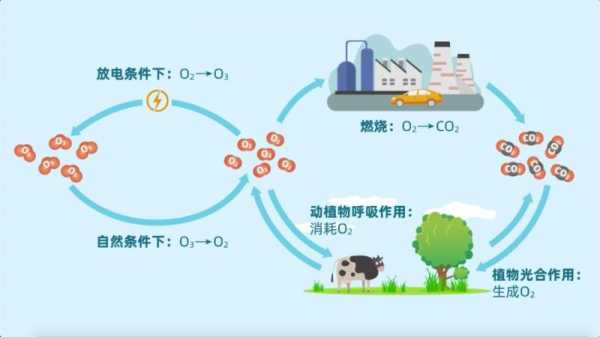
碳循环中碳由生物群落进入无机环境过程伴随能量流动。碳由生物群落进入无机环境一般通过消费者或分解者的呼吸作用。在此过程中,储存在有机物中的化学能转变为供生物生命活动的ATP中的化学能和热能(热能散失)。
等温过程和循环过程的内能变化吗?
理想气体等温过程内能不变化,一个循环过程,内能变到原来的大小。
理想气体在等温变化时,体积发生改变时要做功,与外界发生热量交换,内能不改变。对于一定量物质构成的系统,通过做功、热传递与外界交换能量,引起系统状态变化,而导致内能改变,其间的关系由热力学第一定律给出。
理想气体从状态a开始循环回到状态a的过程是一种等温过程,因此系统不会产生净热量的吸收或放出,即热量不会发生变化。
在等温过程中,气体的温度保持不变,因此它的内能也保持不变。因为内能等于气体的热能加上势能和动能,而温度保持不变,所以热能也不会发生变化。
问题出在能量守恒理解上,Q=CdT说明吸放热都用于内能变化,即用于温升,而没有顾及吸热还可用于做功。由于这里(等温)说明,吸收的热全部用于做功,从而内能不变。
到此,以上就是小编对于循环过程可逆吗的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏