本篇目录:
刚性容器里的水加热,使其在恒温过程中蒸发这个是可逆过程吗_百度...
所以,在水加热的过程中,会有微少的气泡从容器底部冒出来,但是在水沸腾以前,这些溶解的气体几乎已经完全溢出,所以,水开时,气泡中就剩下水蒸气了。
水恒温可逆蒸发下的功是指,当水以恒定的温度和压力下蒸发时,蒸发所需要的能量等于蒸发后水蒸气再汽化所需要的能量,即水在恒定温度和压力下,蒸发和汽化过程所消耗的能量是相等的。
简单来说:分子就是在不断运动着的……况且“蒸发”的定义并没有说一定要加热,也就是说无论是否有空气流动、加热等条件,蒸发也会进行。
气态-液态):雨,水蒸气与热空气一起上升,在高空遇冷时,水蒸气凝结成雨。升华(固态-气态):放在衣柜里的樟脑丸过一段时间不见了。凝华(气态-固态):灯泡钨丝受热升华,形成钨蒸气,然后在灯泡上凝华成固态钨。
汽化和液化互为可逆过程。当温度处于沸点时,持续吸热就是汽化过程,持续放热就是液化过程。
恒温恒压可逆反应与恒温恒容可逆反应
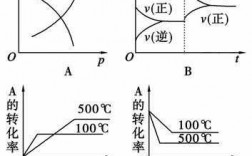
你好:恒压转化率 ≥ 恒容转化率 反应中无气体或气体体积不变,两者一样 有气体,且反应后气体增多。原因:设两者均为恒压,反应平衡后,压缩某一个的体积,使其恒容。
恒温恒容时冲入惰性气体对可逆反应无影响,因为原反应中各气体的分压不变,冲入惰性气体并不会产生什么影响。恒温恒压时冲入惰性气体分两种情况:反应左右系数和相等时,无影响。
等效平衡原理:对于同一个可逆反应,在相同的条件下(恒温恒容或恒温恒压),不管是从正反应开始,还是从逆反应开始,或从正反应和逆反应同时开始,都可以建立同一平衡状态。
.等效平衡 同一可逆反应,一定条件下,当改变起始时反应物或生成物物质的量或物质的量浓度,达到平衡时,混合物中各组分的百分组成相等,这样的平衡称等效平衡。
这两种反应的区别在于有体积变化的反应在恒温恒容的条件下,必然会引起压强变化,压强变化会引起平衡移动,所以不能建立等效平衡而体积不变的反应,就不会引起压强的变化,从而各组分的百分含量不改变。
③平衡后若升高温度,则平衡向 方向移动;若增加压强,则平衡向 方向移动(填“向左”或“向右”)。
《物理化学》中,在哪些情况下△U、△H、△S、△A或△G为零?
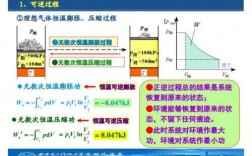
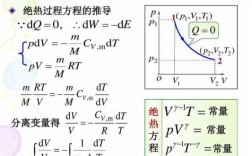
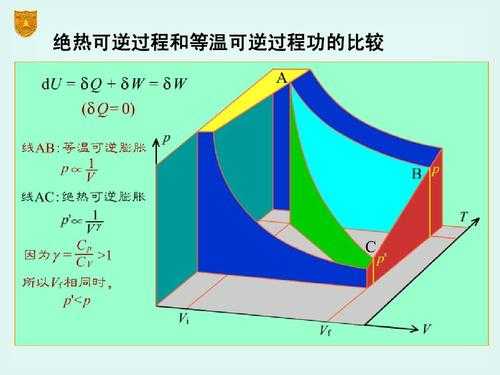
特殊过程(理想气体的循环过程、等温可逆膨胀过程)中△U、△H、△S和△G是等于零。(1)理想气体,恒温过程:△U,△H=0。不可逆过程:△S大于零 ;△A, △G小于零。
△H:吸热为正,放热为负 △S:一般都为非负数,对于封闭体系绝热过程或隔离体系,都大于等于零。其他情况有小于零的时候。△G :一般平衡都是朝着其小于零的方向进行,不可能自动发生△G 0的过程。
q、w、u、h、s、g均为零,因为在正常沸点下蒸发过程中,温度和压强都是恒定的,所以没有任何热量和功的交换,因此 q 、 w 、 u 、 h 、 s 、 g 均为零。
理想气体,恒温过程:△2113U,△H=0。不可逆过程:△S大于零 ;△A, △G小于零 理想气体节流膨胀过程:△H=0,温度不变于是△U=0。
等容过程,dV=0,所以W=0。因为温度是冷却过程 所以U小于0.因为恒容过程,内能变化等于热量,U=Q,Q小于0,放热。S等于nRln(T2/T1)因为放热过程T2大于T1 那么S肯定是大于0的就是不可逆过程。
到此,以上就是小编对于恒温过程g的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏