本篇目录:
- 1、初中化学常见物质溶于水时的吸放热?
- 2、溶解的过程中吸热还是放热?为什么?
- 3、物质溶解在水中为什么会放热或吸热
- 4、物质溶解时,为什么会有吸热或放热的现象
- 5、高中化学:浓酸浓碱溶于水到底是放热还是吸热?有人说浓度大,溶液中阴阳...
初中化学常见物质溶于水时的吸放热?
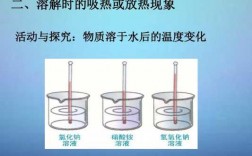
1、溶于水放热的常见物质有:浓硫酸(HSO)、氢氧化钠固体(NaOH)、氧化钠(NaO)、氧化钙(CaO)等。溶于水吸热的常见物质有:硝酸铵(NHNO)、氯化铵(NHCl)等。
2、溶于水吸热:硝酸氨等 吸放热主要是改变了大气压,温度升高大气压降低。所以放热端液面上升,吸热端液面下降。
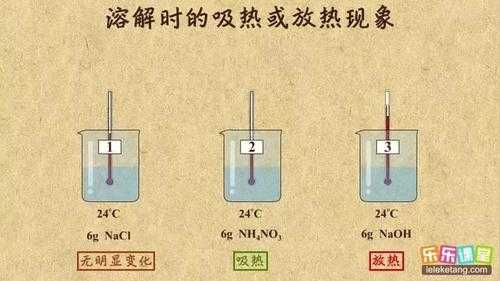
3、.放热反应 ①活泼金属置换水或酸中氢的反应,如:2na+2h2o=2naoh+h2↑ 2al+6hcl=2alcl3+3h2↑ ②酸碱中和反应。
4、放热:浓硫酸、氢氧化钠固体溶于水可放热;与水反应的碱性氧化物(CaO、BaO、K2O、Na2O等)放入水中可放热。甲醇、乙醇,丙酮等有机物溶于水也放热。硝酸铵,硝酸钠,亚硝酸钠等溶于水可吸热 。
5、浓硫酸、固体氢氧化钠、生石灰溶于水放热,硝酸铵吸热,氯化钠基本不变。
6、降温:硝酸钾(KNO3)、硝酸铵NH4NO3(吸热而降温),易溶于水,溶水时吸热、易吸湿和结块,产品一般制成颗粒状。主要用途:用作分析试剂、氧化剂、致冷剂等 升温:硫酸H2SO4。
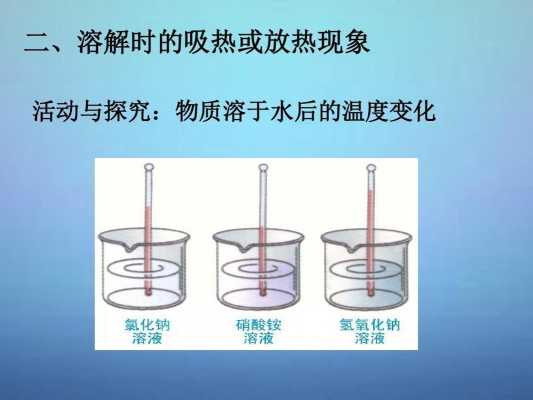
溶解的过程中吸热还是放热?为什么?
成溶剂(水合)分子(或水合离子)的过程,这种过程是化学过程,放出热量。
溶解是水合过程和电离两个同时进行的过程,其中水合过程是放热的,电离过程是吸热的;浓酸浓碱溶解时的水合过程大于电离过程,所以整体表现为放热。
溶解的热效应主要由断裂化学键和离子水合决定,前者吸热而后者放热,差值决定了总的热效应。
这是一个吸热过程。另一个过程为脱离后的分子或离子被溶剂化的过程,这个过程是放热反应。物质溶于溶剂是吸热还是放热,取决于这两个过程那一个占优势。溶剂化过程占优势将溶解放热,扩散过程占优势将是溶解吸热。
溶解过程如果需要热量,首先要吸取溶液中的热量,使溶液降温;溶液过程如果是放出热量,当然首先向溶液中放热,使溶液升温。溶液降温或升温后一定会对外吸热或放热,以达到平衡。当然这是化学反应之后的事情了。
物质溶解在水中为什么会放热或吸热
因为冰点降低,所以,烧杯里面只要有冰和水,那么冰水混合物的问题肯定低于0度,这说明在试管里面完全冻冰之前,热量传输一只会进行下去 2) 让食盐放入装有冰的烧杯内,食盐会另水的冰点下降,造成冰的融化。
因为物质溶于水很多时候仅作为物理变化,实际上很多时候有水合作用发生。另外,即使没有,物质的扩散也需要热量,所以根据物质不同会产生不同的效果。
第一步是物质在水分子的作用下电离水解,生成离子。第二步是离子于水分子结合生成水合离子。其中第一步吸热,第二步放热。有的物质(如浓硫酸)第一步吸收的热量小于第二步放出的热量,所以溶于水放热。
物质溶解时,为什么会有吸热或放热的现象
1、因为物质溶于水很多时候仅作为物理变化,实际上很多时候有水合作用发生。另外,即使没有,物质的扩散也需要热量,所以根据物质不同会产生不同的效果。
2、有的物质(如浓硫酸)第一步吸收的热量小于第二步放出的热量,所以溶于水放热。有的物质(如氯化钠)一,二步吸收放出的能量差不多,表现为不放热也不吸热。有的物质(如硝酸铵)第二步小于第一步,表现为吸热。
3、水合过程,不到大学不会深入研究。物质的溶解过程不单单是物理过程,而是物理——化学过程,在分撒之后,离子会喝水结合变成水喝离子,故此有吸热放热之分。可自行查阅人教版高中教材选修四。
高中化学:浓酸浓碱溶于水到底是放热还是吸热?有人说浓度大,溶液中阴阳...
放热:浓硫酸、氢氧化钠固体溶于水可放热;与水反应的碱性氧化物(CaO、BaO、K2O、Na2O等)放入水中可放热。甲醇、乙醇,丙酮等有机物溶于水也放热。 硝酸铵,硝酸钠,亚硝酸钠等溶于水可吸热 。
反之,当放热多于吸热,紶粻官救擢嚼规楔海盲例如浓硫酸溶解在水里的时候,因为它和水分子生成了相互稳定的化合物,放出的热量多于吸收的热量,就表现为放热,所以溶液的温度显著升高。
反之,当放热多于吸热,例如浓硫酸溶解在水里的时候,因为它和水分子生成了相互稳定的化合物,放出的热量多于吸收的热量,就表现为放热,所以溶液的温度显著升高。
碳酸钠溶于水破坏的氢键是碳酸氢钠的两倍,碳酸钠溶于水放热较多。物质溶于水中发生2个过程,一是水破坏原来物质的化学键(比如碳酸钠溶于水,原来碳酸钠之间的离子键被水破坏),这需要吸收能量。
酸碱溶于水一般放热,典型的是浓硫酸和氢氧化钠。硝酸铵溶于水吸热。记住这三个例子基本就够用了。
状态:浓硫酸是无色黏稠油状液体,稀硫酸没有黏性,两瓶溶液用手摇动,有黏稠感的是浓硫酸;溶于水放热:浓硫酸溶于水会放出大量的热,而稀硫酸没有放热现象。
到此,以上就是小编对于溶质溶解过程放热还是吸热的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏