本篇目录:
- 1、粗盐变成精盐要什么步骤?
- 2、初三化学中粗盐的提纯的步骤是什么,要注意什么
- 3、粗盐提纯所涉及的所有化学方程式
- 4、某化学学习小组用某种粗盐进行提纯实验,步骤如下图所示:请回答:(1...
- 5、...实验室中粗盐提纯的操作步骤如下:(1)将粗盐研细,加水使
粗盐变成精盐要什么步骤?
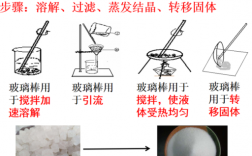
1、粗盐提纯的4个步骤:溶解、过滤、蒸发、转移。粗盐提纯,即将盐中所含有的杂质提取出来,从而制得纯净的盐。而粗盐提纯是我国化学学科中的重要课题。
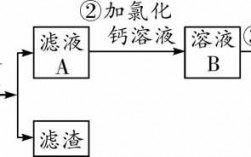
2、粗盐提纯为精盐需要的工艺包括:溶解、沉淀、过滤、除杂、蒸发。将粗盐进行溶解、沉淀,并把其中的不溶物质过滤掉,为了得到更纯净的食盐,还要加入BaCl2等溶液,随后再次过滤,将得到的液体进行蒸发即可以得到精盐。

3、粗盐提纯步骤 先将粗盐溶于水,再过滤(注意一贴二低三靠),该步骤过滤泥沙等不溶性杂质。
初三化学中粗盐的提纯的步骤是什么,要注意什么
1、步骤:溶解、过滤、蒸发结晶,经过这几步操作后除去的是不溶性杂质。
2、答案为:溶解、过滤、蒸发,烧杯、玻璃棒、漏斗、蒸发皿、酒精灯、铁架台。
3、l 蒸发时要经常用玻璃棒搅拌液体,防止由于局部温度过高造成液滴飞溅。l 当水接近全部蒸发时熄灭酒精灯,停止加热,利用余热使剩余水分蒸发。
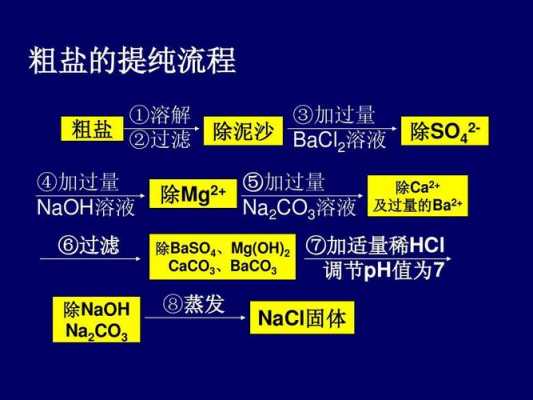
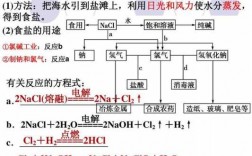
粗盐提纯所涉及的所有化学方程式
1、HCl+Na2CO3==2NaCl+H2O+CO2↑ 蒸发溶液,析出NaCl晶体。
2、溶解:在天平上称量剩下的粗盐,计算在10毫升水中大约溶解了多少克粗盐。加入过量BaCl,目的:去除硫酸根离子。
3、除去粗盐中的硫酸镁,采用的是加入氯化钡,生成不溶于水的硫酸钡,除去硫酸根离子。再加入氢氧化钠,生成不溶于水的氢氧化镁,除去镁离子的方式。
4、粗盐中含有泥沙等不溶性杂质,以及可溶性杂质如:Ca2+,Mg2+,SO42- 等。不溶性杂质可以用过滤的方法除去,可溶性杂质中的Ca2+,Mg2+,SO42-则可通过加入BaClNaOH和Na2CO3溶液,生成沉淀过滤而除去。
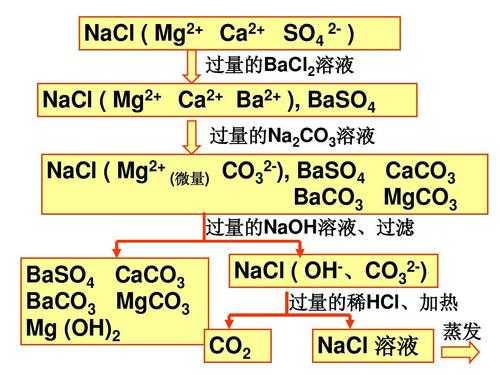
5、在天平上称量剩下的粗盐,计算在10毫升水中大约溶解了多少克粗盐。
6、粗食盐中含有不溶性和可溶性的杂质(如泥沙和K+、Mg2+、SO42+、Ca2+离子等)。不溶性的杂质可用溶解、过滤的方法除去;可溶性的杂质则是向粗食盐的溶液中加入能与杂质离子作用的盐类,使生成沉淀后过滤以除去。
某化学学习小组用某种粗盐进行提纯实验,步骤如下图所示:请回答:(1...
1、(1)蒸发 (2)5 烧杯 (1)根据图示,首先将粗盐加水溶解,再过滤除去泥沙,将滤液蒸发结晶得到氯化钠晶体。
2、溶解 用托盘天平称取5克粗盐(精确到0.1克).用量筒量取10毫升水倒入烧杯里。过滤 按照化学实验基本操作6所述方法进行过滤.仔细观察滤纸上的剩余物及滤液的颜色.滤液仍浑浊时,应该再过滤一次。
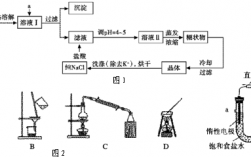
...实验室中粗盐提纯的操作步骤如下:(1)将粗盐研细,加水使
一,加水溶解粗盐 二,静置沉淀 三,将上层清夜倒入漏斗过滤 四,将滤液置于蒸发皿中,加热蒸发 这是简单处理,得到的盐晶体还需进一步提纯(粗盐中一般含有很多杂质离子化合物以及卤素单质或化合物)。
溶解 用托盘天平称取2克粗盐(精确到0.1克)。用量筒量取10毫升水倒入烧杯里。用药匙取一匙粗盐加入水中,并用玻璃棒搅拌;接着再加入粗盐,边加边用玻璃棒搅拌,一直加到粗盐不再溶解时为止。
操作方法及现象:(1)溶称取约4g粗盐加到盛有约12mL水的烧杯中,边加边用玻璃棒搅拌,直至粗盐不再溶解为止 固体食盐逐渐溶解而减少,食盐水略显浑浊。
粗盐提纯步骤如下:先将粗盐溶于水,再过滤(注意一贴二低三靠),该步骤过滤泥沙等不溶性杂质。
粗盐提纯的操作流程:先将粗盐溶于水,再过滤(注意一贴二低三靠),该步骤过滤泥沙等不溶性杂质。
粗盐提纯实验步骤如下:溶称:取约4g粗盐加到盛有约12mL水的烧杯中,边加边用玻璃棒搅拌,直至粗盐不再溶解为止,固体食盐逐渐溶解而减少,食盐水略显浑浊。
到此,以上就是小编对于粗盐提纯过程如下说明的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏