本篇目录:
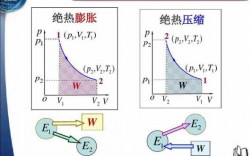
绝热过程的三个公式
1、绝热过程的三个公式:PdV+VdP=nRdT,dQ=dU+dW=0,dU=nCvdT。绝热方程是利用热力学第一定律和理想气体状态方程在准静态条件下导出的,绝热方程的应用必须满足理想气体条件和准静态条件。
2、绝热过程三个公式介绍如下:PdV+VdP=nRdT、dQ=dU+dW=0、pV^(Cp/Cv)=const。绝热过程是一个绝热体系的变化过程,绝热体系为和外界没有热量和粒子交换,但有其他形式的能量交换的体系,属于封闭体系的一种。
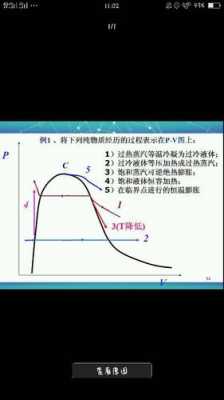
3、公式如下图:关于理想气体,有可逆绝热过程方程,在满足理想气体、绝热、可逆这三个基本条件,才能使用该方程。
4、方程绝热可逆过程:Q=0,△U=W=-P外dV(恒外压);或△U=nCv,mdT;△H=nCp,mdT。定义 绝热可逆:关于理想气体,有可逆绝热过程方程,在满足理想气体、绝热、可逆这三个基本条件,才能使用该方程。
5、mA+nB=xC+yD。化学反应而言,反应物和产物都处于标准状态下,绝热反应过程中的熵变计算公式为mA+nB=xC+yD。熵变的标准计算方法是设计为一个等温过程加一个等压过程。
6、理想气体有ΔU=nCv,m(T2-T1),绝热过程有 ΔU=W,则nCv,m(T2-T1)=-p外(V2-V1)=-p外(nRT2/p2-V1)。据此求出T2,进而求出V2,代回功的表达式即可。其中Cv,m=5/2 R。如有不明,请追问。

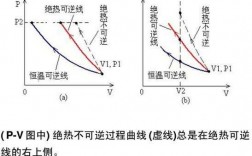
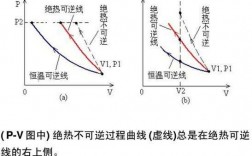
绝热不可逆过程为什么不能存在P-V图上
如果起点一样其他位置不可能相交,因为绝热过程,一个变化过程只对应唯一的末态,在绝热过程中,不可能存在在同一起点经过两个不同过程到达相同末态。如果起点不一样可能会有且只有一个交点。
不可能,可逆过程的每个中间状态都是平衡态(或无限趋于平衡态),有确定的p-V,可以在图上用点表示,可逆过程的图示就是这些点的集合(一条曲线)。
绝热可逆过程就是要求保证你在p-v图上画的那条线上每一点(也就是在过程中任何一个状态)都满足你写的那个式子,而不是只选取两个状态点满足就可以了。
是的,非可逆过程,体系内部压强和环境对其施加压强可能不相等,而PV图的压强指的是内部压强,膨胀功需要外部压强计算。
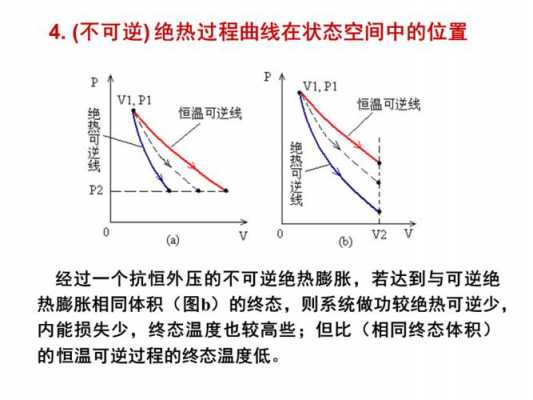
理想气体绝热自由膨胀过程是非准静态过程,除初、末态外,系统每一时刻都处于非平衡态。所以理想气体绝热自由膨胀过程不能用PV图表示。准静态过程PV图曲线下面积等于做功的说法不成立。
无法简单判断。P-V主要是对等压或等容过程的判断,而T-s图则是对等温与等熵(可逆绝热)过程的判断。但是如果知道P-V图中的两条曲线就是等温和等熵线的话,那么更倾斜的那条曲线,一定就是等熵(可逆绝热)线。
绝热情况下pv图与自由度有关吗
绝热自由膨胀过程中,压强、体积两个量的变化关系的确与等温膨胀中这两个量的变化关系相同,即P2V2=P1V1。定压热容与定体热容的比值称为摩尔热容比,用符号γ表示,大小等于(i+2)/i,其中i是理想气体的自由度。
描述状态变化:PV图能够清晰地表示气体的状态变化,包括等温过程、等容过程、等压过程和绝热过程等。通过观察PV图的曲线特征,可以识别和描述气体在不同状态之间的变化。
v2等于2^1/7:1,答案选D 这题画pv图更容易一些,先是做绝热膨胀,然后等压膨胀,最后等温收缩(注意绝热过程比等温过程的图线更陡),根据图像可知这是一个逆循环,它对外界做负功,放出热量,答案选A。
理想气体绝热可逆过程方程
对于理想气体,等温可逆过程,△U=△H=0,W=-nRTlnV2/V1,Q=-W。绝热可逆过程:Q=0,△U=W=-P外dV(恒外压)或△U=nCv,mdT,△H=nCp,mdT。可逆过程是指热力学系统在状态变化时经历的一种理想过程。
方程 对于理想气体,等温可逆过程△U=△H=0;W=-nRTlnV2/V1,Q=-W 绝热可逆过程:Q=0,△U=W=-P外dV(恒外压);或△U=nCv,mdT;△H=nCp,mdT。
对于理想气体,等温可逆过程△U=△H=0,W=-nRTlnV2/V1,Q=-W 绝热可逆过程:Q=0,△U=W=-P外dV(恒外压)或△U=nCv,mdT,△H=nCp,mdT 绝热可逆膨胀:物体的温度可是要变化的。
理想气体可逆绝热过程方程 22 11 其中=热过程。
等温可逆膨胀,变化慢到足以靠与外界的热交换来保持恒温。
方程:P1V1^γ=P2V2^γ是理想气体可逆绝热过程方程!而理想气体绝热自由膨胀过程是不可逆的,熵是增大的,所以不适用上式,所以D错误。
到此,以上就是小编对于绝热过程pv=c的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏