本篇目录:
- 1、一定质量的某种理想气体分别经历如图所示的三种变化过程,其中表示等压...
- 2、如图所示理想气体经过abca
- 3、有一理想气体从一状态开始,使其体积膨胀为原来的二倍,经历了三个过程...
- 4、等容加热时,一摩尔理想气体经历的过程
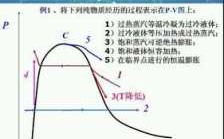
一定质量的某种理想气体分别经历如图所示的三种变化过程,其中表示等压...
(1)pdV= (M/ Mmo)RdT表示等压过程。(2) Vdp= (M/ Mmo)R dT表示等体过程。(3)pdV+Vdp=0表示等温过程。
对本题作 p - V 图线如图所示,气体从 A 状态经过一个循环回到状态 A 。
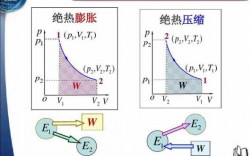
所以等压过程内能增加多;等温膨胀压强要减小,对外做功等于压强乘以体积变化,本题体积变化相同,但等温膨胀压强要减小,所以等温膨胀平均压强小于等压膨胀过程,等压膨胀过程对外做功。
再看,由于等压过程中压力不变,而体积增大,那么气体的内能一定增加了,这在p-V图上可以直接看出来。定量地说,气体的温度会上升为原来的两倍。绝热过程中气体和外界没有热传递,一切变化由做功实现。
你这句话说得有问题吧。这个题目不是说对某一个过程,把它的做功和热量比较。而是将等温过程、等压过程、绝热过程这三个过程的做功进行比较,传热也进行比较。等温过程怎么将温度增加一倍?请采纳答案,支持我一下。
如图所示理想气体经过abca
1、mol双原子理想气体,始态为200kPa、12dm3,经pT=常数的可逆过程(即过程中pT=常数)压缩到终态为400kPa。
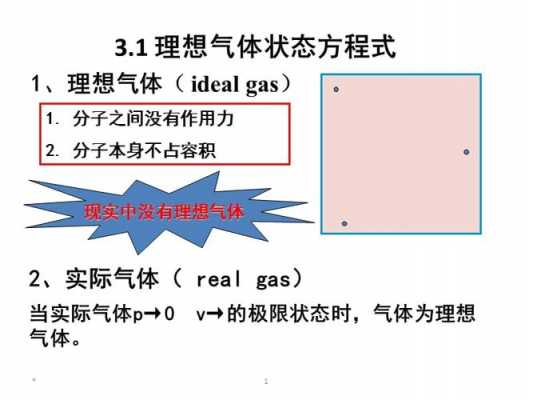
2、CD过程是等温减压增容即等温膨胀,DA过程是等压降温减容即等压压缩。已知V A =1L,V B =1L(等容过程)由 (等压过程)得: L由(等温过程) 得: L所改画的p一V图如图所示。
3、+1/2 (p+4p)(4V-V)=3Cv pV/nR+5pV 5 一个循环净功W=5pV 6 效率=W/Q,此处的Q为A-B过程吸热量,带入即可。注:Cv=5nR,Cp=5nR,由双原子分子理想气体得知。如有不明欢迎追问。
4、abc是等温过程,adc与abc不重合,所以adc不是等温过程。A错 ac温度相同,则内能相同。而abc和adc两个过程对外做功不同,所以吸收热量不同。
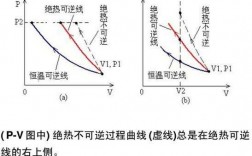
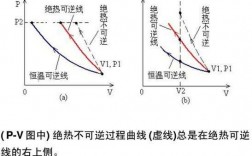
有一理想气体从一状态开始,使其体积膨胀为原来的二倍,经历了三个过程...
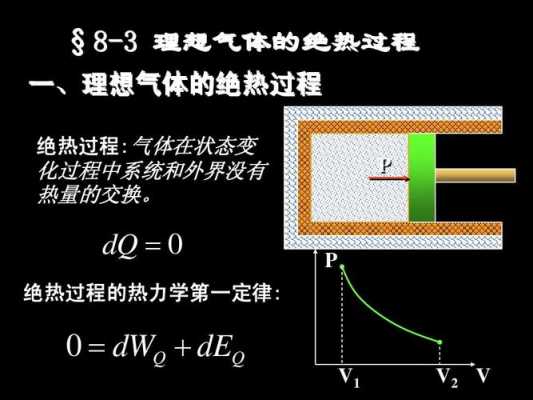
答案AC. 对于AB等压过程,体积膨胀,气体对外做功,内能减少,放热。对于AD过程,绝热,没有热量交换。AC过程气体对外做的功等于吸热。
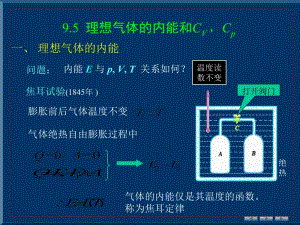
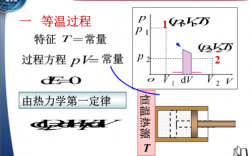
:理想气体等温膨胀,温度不变,气体的内能不变。2:在等温膨账的过程中,吸收外界的热量全部转换为对外作功。3:由于V1扩到V2,无具体数据,所以不能定量计算。
自由膨胀过程 由于体系经历绝热过程,故与外界无热交换。又由于气体向真空自由膨胀,外压为零,故体系对环境做功也为零。
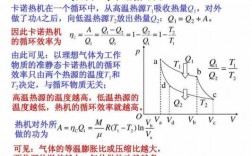
等容加热时,一摩尔理想气体经历的过程
1、如果是可逆等温过程,则: Q=TΔS=T(S2-S1),W=Q-ΔU=TΔS-ΔU式中S为系统的熵。如果是理想气体的等温膨胀(或压缩)过程,系统的状态变化满足pV=常数。
2、等容变化;加热气体,气体温度升高,则内能增大,即内部分子的热运动加剧,对容器[容积不变]壁碰撞就剧烈,压强增大。反之压强减小。
3、第一过程为等容过程,所以V1=V2,等容过程不做功。
到此,以上就是小编对于某理想气体反应过程的∑νbg=2的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏