本篇目录:
- 1、等温条件下系统做功和吸收热量公式
- 2、理想气体等温过程中的做功方程式如何写出?
- 3、经过等压,等温或绝热过程膨胀相同体积,做功最多的是什么过程
- 4、等温可逆膨胀做的功怎么计算
- 5、等温过程的功是怎样的?
等温条件下系统做功和吸收热量公式
等温过程气体对外做功公式:U=U1+U2。等温过程是热力学过程的一种,即是指热力学系统在恒定温度下发生的各种物理或化学过程。在整个等温过程中,热量的传递使系统与其外界处于热平衡状态。
吸收热量的公式为:吸收热量=物质的质量×物质的比热容×温度变化。吸收热量公式的定义 吸收热量公式是热力学能(内能)的变化量与吸收的热量成正比,与热传递的方向相反。

热力学常见定律与公式:第一定律:△U=Q-W。△U是系统内能改变,Q是系统吸收的热量,W是系统对外做功。第二定律:很多种表述,最基本的克劳修斯表述和开尔文表述。
理想气体等温过程中的做功方程式如何写出?
1、等温过程气体对外做功公式:U=U1+U2。等温过程是热力学过程的一种,即是指热力学系统在恒定温度下发生的各种物理或化学过程。在整个等温过程中,热量的传递使系统与其外界处于热平衡状态。
2、等温可逆膨胀功的公式是:对于理想气体,等温可逆过程:△U=△H=0,W=-nRTlnV2/V1,Q=-W。气体吸收的热量就等于气体对外所做的功。
3、理想气体状态方程可用pV=nRT表示,式中:p为压强(Pa),V为气体体积(m),T为温度(K),n为气体的物质的量(mol),R为摩尔气体常数(也叫普适气体恒量)J/(mol.K。

经过等压,等温或绝热过程膨胀相同体积,做功最多的是什么过程
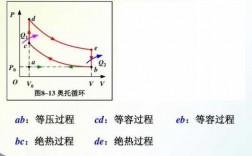
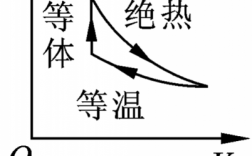
1、请你将这三个过程,画在同一P—V图上,再进行比较所围面积,可知等压做功最多,其次是等温,最是绝热。
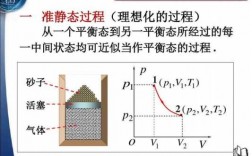
2、等温膨胀:所谓等温膨胀就是指一定质量的理想气体在温度不变的条件下缓慢进行的膨胀过程.可见等温膨胀是准静态过程。特征:温度不变,体积增大。
3、所以等压过程内能增加多;等温膨胀压强要减小,对外做功等于压强乘以体积变化,本题体积变化相同,但等温膨胀压强要减小,所以等温膨胀平均压强小于等压膨胀过程,等压膨胀过程对外做功。
4、等温过程,由热力学定律(忘了那一条),体积膨胀,温度会降低,。

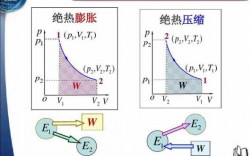
5、绝热膨胀过程,和外界没有热交换,对外做功,则内能减小,温度降低,压强减小,做功F=∫PdV,所以显然等温过程对外做功多。
等温可逆膨胀做的功怎么计算
对于理想气体,等温可逆过程,△U=△H=0,W=-nRTlnV2/V1,Q=-W。绝热可逆过程:Q=0,△U=W=-P外dV(恒外压)或△U=nCv,mdT,△H=nCp,mdT。可逆过程是指热力学系统在状态变化时经历的一种理想过程。
等温可逆膨胀功的公式是:对于理想气体,等温可逆过程:△U=△H=0,W=-nRTlnV2/V1,Q=-W。气体吸收的热量就等于气体对外所做的功。
等温可逆膨胀,体系对环境做最大功。熵是状态函数,只与其实状态有关。
等温过程的功是怎样的?
1、简单地说就是在理想气体的等温过程当中,当气体膨胀,对外作功和吸收的热量都是正的。同时气体从恒温热源吸收的热量,完全用于对外做功。等温过程最重要的是,内能变化为零。、 这样吧,我给你看一道例题,把等温等压等容绝热联系起来。
2、三种过程系统环境的功和热分别是等压过程、等温过程、绝热过程。等压过程(也称为等容过程):在等压过程中,系统保持恒定的压强,但体积可以改变。此时,系统对环境做功的大小等于PΔV,即系统的压强乘以体积变化量。
3、等温过程气体对外做功公式:U=U1+U2。等温过程是热力学过程的一种,即是指热力学系统在恒定温度下发生的各种物理或化学过程。在整个等温过程中,热量的传递使系统与其外界处于热平衡状态。
4、等温可逆膨胀功的公式是 对于理想气体,等温可逆过程:△U=△H=0,W=-nRTlnV2/V1,Q=-W。气体吸收的热量就等于气体对外所做的功。可逆过程是指热力学系统在状态变化时经历的一种理想过程。
到此,以上就是小编对于等温过程气体做功用气体的压强还是外界压强pdf的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏