本篇目录:
磷的气态氢化物的形成过程,最高价氧化物对应的说化物与naoh反应能生成几...
三种,要看量的多少,是否过量等(因为磷酸是三元弱酸,会发生三级电离),非别为磷酸钠(Na3PO4),磷酸氢钠(Na2HPO4),磷酸二氢钠(NaH2PO4)。
磷的最高价氧化物是P2O5,对应的水化物是磷酸H3PO4,磷酸是3元酸,一个H3PO4分子可以电离出3个H+,所以磷酸与一元强碱NaOH反应,能生成3种盐,分别是磷酸一氢钠Na2HPO4,磷酸二氢钠NaH2PO4,磷酸钠Na3PO4。

∴最高价氧化物为五氧化二磷(P2O5 别名:磷酸酐 )遇水能发生大量烟雾和热量,遇潮时,对大多数金属有轻微的腐蚀性。磷酸(H3PO4)是三元中强酸,分三步电离,不易挥发,不易分解,几乎没有氧化性。
磷的最高价氧化物对应的水化物是磷酸,一定能与强碱(如氢氧化钠溶液)发生中和反应。
如何判断PH3和NH3的杂化类型?
NH的杂化轨道类型是sp杂化。同一原子内由一个ns轨道和三个np轨道发生的杂化,称为sp杂化,杂化后组成的轨道称为sp杂化轨道。sp杂化可以而且只能得到四个sp杂化轨道。
杂化类型是sp3杂化。PH3分子中的磷原子采用sp3杂化。磷化氢分子构型与氨分子相同,呈三角锥形。
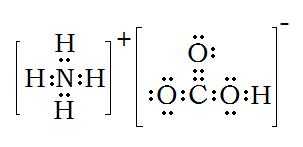
NH3的杂化轨道类型是SP3;(1)sp杂化 同一原子内由一个ns轨道和一个np轨道发生的杂化,称为sp杂化。杂化后组成的轨道称为sp杂化轨道。sp杂化可以而且只能得到两个sp杂化轨道。
磷化氢的电子式是啥啊?
ph3的结构式和电子式,结构式为P,与NH3的结构类似,呈三角锥形。根据查询相关资料信息显示:PH3电子式:H..P:H..H在化学反应中,一般是原子的外层电子发生变化。
电子式 H:C┇┇C:H乙炔分子量 204 ,气体比重 0.91(kg/m3),火焰温度3150 ℃,热值12800(kcal/m3)在氧气中燃烧速度 5 ,纯乙炔在空气中燃烧2100度左右,在氧气中燃烧可达3600度。
个sp3杂化轨道中填充了3个σ键的成键电子对和1个未成键价电子对,使得分子的空间构型为三角锥形。ph3特点:磷化氢是一种无色、剧毒、易燃的储存于钢瓶内的液化压缩气体,化学式为PH3。
白磷能直接与卤素、硫、金属等起作用,与硝酸生成磷酸,与氢氧化钠或氢氧化钾生成磷化氢及次磷酸钠。应避免与氯酸钾、高锰酸钾、过氧化物及其他氧化物接触。白磷和红磷的区别是在于着火点和毒性,白磷着火点低于红磷。
英文别名:Phosphonic acid; hydrogen phosphonate;[1] phosphorus(+3) trihydride cation trihydroxide 分子式:H3PO3分子量:800 外观:无色晶体。
到此,以上就是小编对于ph 3的电子式形成过程的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏