本篇目录:
- 1、绝热或封闭系统,不可逆过程是熵增
- 2、我们谈论的不可逆过程的“熵变”是什么?
- 3、不可逆的过程熵一定为0吗?
- 4、工质经历一个不可逆放热过程后,熵怎么变
- 5、不可逆过程的熵如何计算
- 6、不可逆过程中,系统与环境的熵变分别是怎么变化的?
绝热或封闭系统,不可逆过程是熵增
1、熵判据的使用条件是在封闭且绝热的系统中;吉布斯函数判据的使用条件是在恒温、恒压、不做非体积功的条件下。
2、应该改成:系统的熵在可逆绝热过程中不变,在不可逆绝热过程中单调增大。这是熵增加原理。由于孤立系统内部的一切变化与外界无关,必然是绝热过程,所以熵增加原理也可表为:一个孤立系统的熵永远不会减少。

3、在热力学的绝热过程中,如果内能不变那么熵就不会改变。熵,热力学中表征物质状态的参量之一,通常用符号S表示。
我们谈论的不可逆过程的“熵变”是什么?
1、熵变等于热量微源除以T的积分,不可逆大于。对于化学反应而言,若反应物和产物都处于标准状态下,则反应过程的熵变,即为该反应的标准熵变。
2、熵变化为零。因为是循环。不可逆只是说熵产大于零,即不可逆造成的能量耗散大于零。熵的变化量等于熵产加熵流。孤立系统是工质加外界环境组成的。耗散都到外界环境了,所以外界环境熵增。所以孤立系统熵增。
3、比如理想气体扩散后不可能自己缩回去,温度只能自发从高温传到低温,这些都是熵增的过程。一句话,不可逆过程。

不可逆的过程熵一定为0吗?
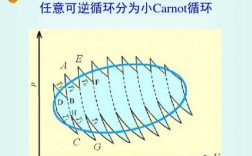
因为熵是状态函数,所以体系熵变为零,其次,因为循环是不可逆的,所以系统加环境的总熵一定大于零,即环境的熵变大于零。对于一个可逆的循环过程,可以分解为很多的微小的循环的积分,在这些微小的循环中熵变为0。
为零。描述工质状态特性的物理量称为状态参数,常用的工质状态参数有温度、压力、比容、焓熵、内能等,基本状态参数有温度、压力、比容。为了能够充分地将热能转换为机械能,要求工质具有良好的膨胀性能。
所以,绝热可逆过程的熵改变为0,但是内能改变不一定为0;而不可逆过程的内能改变为0,但是熵改变一定为正值。
其中总熵变题设为0;绝热流动说明熵流为0;不可逆流动说明熵产0;所以增加的熵加在了质流熵里。(题设为稳定流动,非稳态稳流!所以状态是变化的!!质流熵不能像稳态稳流里一样直接变为0。

不管可逆热机还是不可逆,只要是循环,熵变都是等于零的。
工质经历一个不可逆放热过程后,熵怎么变
1、经过一个循环,工质的终态与初态一致,所以不论何种循环,熵的变化均等于0,即熵值不变。
2、为了能够充分地将热能转换为机械能,要求工质具有良好的膨胀性能。同时为了保证工质连续地流过热力设备而不断地做功,要求工质具有良好的流动性。
3、应该改成:系统的熵在可逆绝热过程中不变,在不可逆绝热过程中单调增大。这是熵增加原理。由于孤立系统内部的一切变化与外界无关,必然是绝热过程,所以熵增加原理也可表为:一个孤立系统的熵永远不会减少。
4、熵变等于热量微源除以T的积分,不可逆大于。对于化学反应而言,若反应物和产物都处于标准状态下,则反应过程的熵变,即为该反应的标准熵变。
5、熵是状态参数不错,熵变就是过程量,过程量等于过程量。熵变是可逆过程热温商,对于不可逆过程应该在不改变始终态前提下设计另一条可逆途径,对于绝热过程,可逆绝热与不可逆绝热不能具有相同始终态。
6、而熵的改变可以通过热力学第二定律来描述,热力学第二定律指出在一个孤立系统中,熵总是要增加的,即△S=0。因此,在绝热可逆过程中,熵的改变为0,即△S=0。
不可逆过程的熵如何计算
熵是状态量,不是过程量。所以熵变与过程无关,于可逆与否无关。不管过程如何,可逆或不可逆,熵变的大小都等于末态熵减去初态熵。不可逆熵变大于0,可逆为0是有前提条件的:绝热。
熵变等于热量微源除以T的积分,不可逆大于。对于化学反应而言,若反应物和产物都处于标准状态下,则反应过程的熵变,即为该反应的标准熵变。
可以先等温可逆变化到n1,P2,T1,V1‘,再等压可逆变到n1,P2,T2,V2’。
不可逆过程中,系统与环境的熵变分别是怎么变化的?
因为熵是状态函数,所以体系熵变为零,其次,因为循环是不可逆的,所以系统加环境的总熵一定大于零,即环境的熵变大于零。对于一个可逆的循环过程,可以分解为很多的微小的循环的积分,在这些微小的循环中熵变为0。
此外因为不可逆循环过程是不可逆的,所以系统加环境的总熵一定大于零,即环境的熵变大于零。
系统熵增加,因为熵流虽然为零,但熵产因为不可逆是大于零的。由于绝热条件,环境不得到热量,因此环境的熵不变化。
熵的变化包括两个部分:一是系统和环境间发生热传导或质量输运,另一部分是由系统内不可逆的热力学过程产生的熵增。如果上述两个部分都不发生,则熵不变。对封闭系统,没有质量输运。对绝热系统,没有热传导。
到此,以上就是小编对于不可逆过程熵变为零吗的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏