本篇目录:
阿司匹林的合成实验流程图
阿司匹林的合成实验流程图如下:1,原料准备:原料包括水、苯甲酸(水杨酸)和乙酸无水乙酯。这些原料需要经过严格筛选和检测,确保品质稳定。2,水杨酸的酯化反应:将苯甲酸和乙酸无水乙酯放入反应釜中,在适当的温度下进行反应。
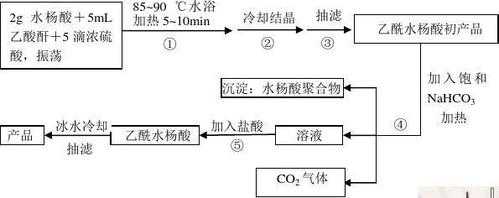
乙酰水杨酸的制备实验装置图如下:制备方法 阿司匹林经水杨酸乙酰化而得:在反应罐中加乙酐(加料量为水杨酸总量的0.7889倍),再加入三分之二量的水杨酸,搅拌升温,在81~82℃反应40~60min。降温至81~82℃保温反应2h。
方程式为 、 。(3)阿司匹林中含有羧基和酯基,但水解后产生的羟基是酚羟基,所以需要消耗3mol氢氧化钠,方程式为 。(4)冷水一方面除去晶体表面附着的杂质,另一方面也减少阿司匹林因溶解而引起的损耗。
阿司匹林经水杨酸乙酰化而得,化学反应方程式如下:制备方法为:在反应罐中加乙酐(加料量为水杨酸总量的0.7889倍),再加入三分之二量的水杨酸,搅拌升温,在81~82℃反应40~60min。降温至81~82℃保温反应2h。
合成阿司匹林的化学反应方程式:阿司匹林经水杨酸乙酰化而得:在反应罐中加乙酐(加料量为水杨酸总量的0.7889倍),再加入三分之二量的水杨酸,搅拌升温,在81~82℃反应40~60min。降温至81~82℃保温反应2h。
实验可以用水杨酸和醋酐来合成乙酰水杨酸(阿司匹林)。过程:实验步骤:在50mL圆底烧瓶中,加入干燥的水杨酸0g(0.050mol)和新蒸的乙酸酐10ml(0.100mol)(思考题1),再加10滴浓硫酸,充分摇动(思考题2)。
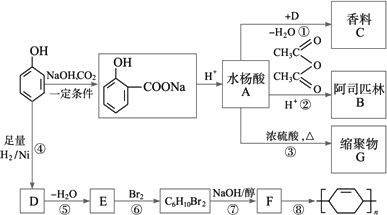
阿司匹林合成过程中浓硫酸作用是什么
因为要发生一个酯化反应,浓硫酸作为催化剂和吸水剂。浓硫酸在这里的作用是脱水剂和吸水剂,一方面脱水作用促进酯化反应,另一方面吸水作用使这种可逆反应向着酯化反应的正方向移动,促进产品的生成。
阿司匹林,是乙酰水杨酸,是由水杨酸和乙酸酐合成的,乙酰水杨酸的合成要发生一个酯化反应,在此反应中浓硫酸作为催化剂和吸水剂。
本品刺激皮肤、黏膜,因能与机体组织中的蛋白质发生反应,所以有腐蚀作用。能使角膜增殖后剥离。其毒性比苯酚弱,但大量服用能引起呕吐、腹泻、头痛、出汗、皮疹、呼吸频促、酸中毒症和兴奋。其水溶液呈酸性反应。
合成乙酰水杨酸时可以不加浓硫酸,不过需要调节反应物。必须使用乙酸酐来发生酰基化反应。在酯化反应中,有两种常见途径,一是反应物酸A 加浓硫酸。二是使用酸A对应的酸酐,可以不用浓硫酸。酸酐的酰基化活性比酸高。

浓硫酸的作用是破坏水杨酸分子中羟基与羟基间形成的氢键,从而使酰化反应较易完成。主反应:在生成乙酰水杨酸的同时,水杨酸分子之间也可以发生缩合反应,生成少量的聚合物。
阿司匹林的制备中重结晶为什么损失大
此外,水杨酸是易溶于水的,不可能是油状物质,出现了油状物质,应该是副产物,比如说一些酯类物质,但是酯一般是无色的,因此该黄色也是三价铁造成的;最后,结晶时搅拌是因为重结晶的时候乙醇加多了,导致析不出晶体。
最后称量过程中由于换滤纸,滤纸上也损失了一部分,更有甚者你不小心弄洒了一些,累计出来产率就低了,做的产率也才百分之五十。
可能是酸加多了,乙酰水杨酸是脂,在酸性条件下会水解,因此得不到结晶。在生成乙酰水杨酸的同时,水杨酸分子间也能发生聚合反应,生成少量聚合物(副产物)。
阿司匹林用水乙醇重结晶与苯重结晶从产品纯度考虑乙醇重结晶更好。乙醇不溶解晶体,减少晶体的损失。有机溶剂中,乙醇的毒性低,苯是一类致癌溶剂。
此步是为了溶解铬盐。 此步是为了除去未作用的对硝基甲苯,此时对硝基甲苯成钠盐溶于水中。 硫酸不能反加于滤液中,这样会使生成的沉淀包含滤液,影响产物纯度。
首先是它并不容易与阿司匹林发生化学反应。其次它在毒性腐蚀性比较小,并且挥发度适中,而且他对阿司匹林的溶解性比较好。它本身的易燃易爆性能也必须过关的,不能是那种非常容易爆燃的东西。
阿司匹林的合成
1、阿司匹林的合成实验流程图如下:1,原料准备:原料包括水、苯甲酸(水杨酸)和乙酸无水乙酯。这些原料需要经过严格筛选和检测,确保品质稳定。2,水杨酸的酯化反应:将苯甲酸和乙酸无水乙酯放入反应釜中,在适当的温度下进行反应。
2、副反应:在生成乙酰水杨酸的同时,水杨酸分子间可发生缩合反应,生成少量的聚合物。乙酰水杨酸能与碳酸氢钠反应生成水溶性钠盐,而其副产物聚合物不能溶于碳酸氢钠溶液。利用这种性质上的差别,可纯化阿司匹林。
3、阿司匹林经水杨酸乙酰化而得,化学反应方程式如下:制备方法为:在反应罐中加乙酐(加料量为水杨酸总量的0.7889倍),再加入三分之二量的水杨酸,搅拌升温,在81~82℃反应40~60min。降温至81~82℃保温反应2h。
4、阿司匹林经水杨酸乙酰化而得:在反应罐中加乙酐(加料量为水杨酸总量的0.7889倍),再加入三分之二量的水杨酸,搅拌升温,在81~82℃反应40~60min。降温至81~82℃保温反应2h。
5、前言:乙酰水杨酸即阿司匹林(Aspirin),是19世纪末合成成功的一种具有解热止痛、治疗感冒作用的药物,至今仍被广泛使用。
阿司匹林制备过程中可能产生的杂质及为何会产生?
有机反应通常都是有或多或少的副反应发生的。因为有机反应的影响因素非常多,反应条件复杂而且设备状况的不同,后处理方式的不同也会以造成不同的杂质。将反应后的内容物抽滤,用少量冰水洗涤两次,得阿斯匹林粗产物。
是因为乙酰水杨酸容易水解所引入的。口服小剂量(1g以下)乙酰水杨酸时,其代谢按一级动力学进行,半衰期约2~3小时。当用量≥1g时,其代谢方式变为零级动力学,半衰期延长至15~30小时,如剂量再增大,可出现水杨酸中毒。
由于酰化反应不完全,使乙酰水杨酸中含有未反应的水杨酸,或因产品贮存不当,水解产生水杨酸。原料残存(生产过程中乙酰化不完全)、水解产生(储存过程中水解产生)。选用的检查方法为对照法。
阿司匹林是以水杨酸为原料,在浓H2SO4的催化下经醋酐乙酰化制得。
【答案】:E 阿司匹林生产过程中乙酰化不完全或贮藏过程中水解产生游离水杨酸。水杨酸在空气中会被逐渐氧化成醌型有色物质(淡黄、红棕、深棕色等),使阿司匹林变色,故需检查。
到此,以上就是小编对于阿司匹林合成过程中浓盐酸加入量是多少毫升的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏