本篇目录:
- 1、滴定分析中有哪些注意事项
- 2、使用滴定管的注意事项
- 3、氯离子的检测硝酸银滴定法,实验过程中应该注意什么事项?
- 4、中和滴定的操作中有哪些注意事项?
- 5、络合滴定法的操作应该注意哪些问题?
- 6、乙酸的电位滴定分析注意事项
滴定分析中有哪些注意事项
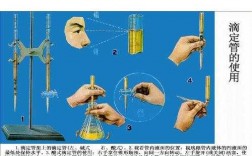
实验注意事项 一 摇瓶时,应微动腕关节,使溶液向一个方向做圆周运动,但是勿使瓶口接触滴定管,溶液也不得溅出。二 滴定时左手不能离开旋塞让液体自行流下。三 注意观察液滴落点周围溶液颜色变化。
摇瓶时,应微动腕关节,使溶液向一个方向做圆周运动,但是勿使瓶口接触滴定管,溶液也不得溅出。滴定时左手不能离开旋塞让液体自行流下。注意观察液滴落点周围溶液颜色变化。

滴入半滴溶液时,也可采用倾斜锥形瓶的方法,将附于壁上的溶液涮至瓶中。这样可避免吹洗次数太多,造成被滴物过度稀释。滴定管的读数 滴定管读数前,应注意管出口嘴尖上有无挂着液滴。
乙酸的电位滴定分析注意事项如下。溶液应按照标准化学实验室操作规范准备,保证溶液的准确性和稳定性。在滴定过程中需要控制滴定速度,一般建议滴定速率不超过每秒2~3滴,以免误差较大。
接近滴定终点时,滴定操作要注意:逐滴加入,每一滴加入后都要充分震荡,否则容易错过滴定终点。
配制硝酸银溶液时,溶剂用蒸馏水不用自来水,防止自来水的氯离子干扰。硝酸银不稳定遇光容易分解,滴定管需要棕色玻璃管 氯离子与银离子反应生成白色沉淀氯化银,氯化银不溶于盐酸、硫酸和硝酸。

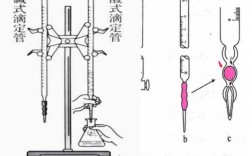
使用滴定管的注意事项
1、(3)读数必须读到小数后第二位,而且要求估计到0.01。(4)为更好地读数,可在滴定管后面衬一读数卡。
2、(1)滴定管使用前必须试漏。方法是:滴定管活栓不涂油脂,注水至全容量,垂直静置15min,所渗漏的水不超过最小分度值,即可使用。(2)向滴定管注入标准液时,应先用少量标准液把滴定管润洗2~3次。
3、滴定管不润洗。——偏大 滴定管尖嘴气泡前无后有。——偏小 滴定管尖嘴气泡前有后无。——偏大 滴定管读数俯视。——偏小 滴定管读数仰视。——偏大 锥形瓶润洗。——偏大 锥瓶摇动外溅。
4、注意事项使用时先检查是否漏液。用滴定管取时必须洗涤、润洗。读数前要将管内的气泡赶尽、尖嘴内充满液体。读数需有两次,第一次读数时必须先调整液面在0刻度或0刻度以下。
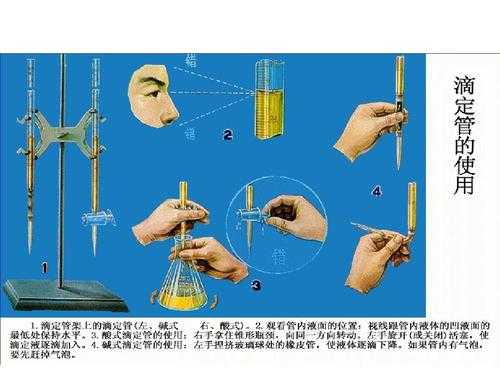
5、滴定管的使用方法及注意事项:使用方法 洗涤。
氯离子的检测硝酸银滴定法,实验过程中应该注意什么事项?
1、测氯离子时判断滴定终点,是用铬酸钾做指示剂,先铬酸钾在银离子很少的情况下为黄色,当滴定到重点,银于离子形式存在时,和铬酸钾结合,此时为砖红色,此滴定是利用电位滴定的原理。
2、配好后应置棕色瓶内,避光保存。②取样品后,迅速分离血浆(清),以免血浆中CO2与红细胞内氯离子发生转移,而使结果偏高。
3、在滴定的过程中,需要控制滴定的速度和时间,以避免出现过滴定或欠滴定的现象。当样品溶液中出现砖红色沉淀时,即可停止滴定。结果计算 在完成滴定操作后,需要对测定结果进行计算。
中和滴定的操作中有哪些注意事项?
二 滴定时左手不能离开旋塞让液体自行流下。三 注意观察液滴落点周围溶液颜色变化。开始时应边摇边滴,滴定速度可稍快(每秒3~4滴为宜),但是不要形成连续水流。
滴定时,要观察滴落点周围颜色的变化。不要去看滴定管上的刻度变化,而不顾滴定反应的进行。滴定速度的控制方面,一般开始时,滴定速度可稍快,呈“见滴成线”,这时为10mL/min,即每秒3~4滴左右。
好几个步骤:1,洗仪器 2,在酸碱管里加溶液 3开始滴定 注意:1,不要把酸液加到碱管里去了 2,滴的时候先快后慢要达到滴定要求是应该控制在3秒/滴 3,滴的时候要摇动滴瓶。
酸碱中和滴定的注意事项:摇瓶时,应微动腕关节,使溶液像一个方向做圆周运动,但是勿使瓶口接触滴定管,溶液也不得溅出。滴定时左手不能离开旋塞让液体自行流下。注意观察液滴落点周围溶液颜色变化。
接近滴定终点时,滴定操作要注意:逐滴加入,每一滴加入后都要充分震荡,否则容易错过滴定终点。
酸碱中和滴定的操作步骤和注意事项可用口诀来概括: 酸管碱管莫混用,视线刻度要齐平。 尖嘴充液无气泡,液面不要高于零。 莫忘添加指示剂,开始读数要记清。 左手轻轻旋开关,右手摇动锥形瓶。
络合滴定法的操作应该注意哪些问题?
强碱滴定弱酸: 如NaOH滴定HAc 突跃范围PH 74-7 ,计量点PH72 。选碱性范围指示剂酚酞、百里酚酞。不能用酸性指示剂甲基红,甲基橙。
,ph=10的时候,钙镁离子可以与edta反应,会使测定的结果偏大,而当ph=5~6的时候,由于酸效应的影响,钙镁离子不能和edta结合形成稳定的化合物,所以对结果无影响。2,不能。
对于稳定性高的络合物,溶液的pH值即使稍低一些,仍可进行滴定,而对稳定性差的络合物,若溶液pH值降低,就不能滴定。
在化学分析中经常利用金属离子与某些试剂生成配合物的反应来测定样品中某些金属离子的含量。而这种利用形成配合物或络合物反应进行的滴定分析法,被称为络合滴定法,也称为配位滴定分析法。
问题1,合适的ph值,你可以查EDTA络合Zn的酸度系数,好像是6左右。
乙酸的电位滴定分析注意事项
1、注意事项 (1)温度:温度变化对滴定介质冰醋酸影响较大,冰醋酸的凝点为16℃,当室温低于16℃,单一气体检测仪滴定液就会凝聚在滴定管中,因此滴定温度应控制在20℃以上。
2、实验目的:通过醋酸的电位消定,掌握电位消定的基本操作、PH的变化及指示剂的选择。学习食用醋中醋酸含量的测定方法。实验原理:食用的主要酸性物质是醋酸(HAC),此外还含有少量其他的弱酸。
3、滴定分析中对化学反应的主要要求是什么?溶液中进行的不可逆或者正反应速率远大于逆反应速率的反应 要有数值上的突跃。
到此,以上就是小编对于滴定基本操作注意事项的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏