本篇目录:
绝热膨胀温度变化
绝热膨胀温度会降低。分析:因为绝热自由膨胀后,δQ=0,δW=0,dU=0。由于是范德华气体,膨胀后气体体积增加导致气体分子间势能增大,而dU=0,所以气体平均动能必然降低,温度下降。
热膨胀过程中气体的温度变化规律是气体温度随热膨胀程度的增大而增大。在热膨胀过程中,气体的体积随温度的升高而增大,同时气体的质量保持不变,因此气体的密度随温度的升高而减小。
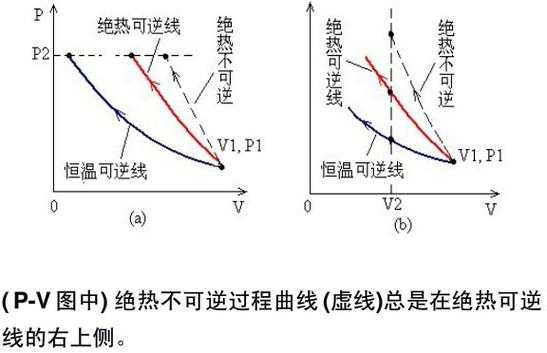
真实气体自由膨胀,温度可能升高,降低或不变。自由膨胀即反抗真空膨胀,W=0。绝热过程Q=0。所以根据热力学第一定律,气体的ΔU=0。以上结论,不管气体是理想气体还是真实气体,均成立。
温度会降低,因为绝热自由膨胀后,δQ=0,δW=0,dU=0.由于是范德华气体,膨胀后气体体积增加导致气体分子间势能增大,而dU=0,所以气体平均动能必然降低,温度下降。
绝热变化时,虽然空气团跟外界没有热量交换,但是由于外界压强的变化使其压缩或向外膨胀,温度也会发生变化。
温度会降低,因为绝热自由膨胀后,δQ=0,δW=0,dU=0.由于是范德华气体,膨胀后气体体积增加导致气体分子间势能增大,而dU=0,所以气体平均动能必然降低,温度下降。真实气体在自由膨胀时会有温度的变化。
什么是绝热温升
1、对于失控体系,反应物完全转化时所放出热量导致物料温度升高,称为绝热温升。绝热温升与反应放热量成正比,对于放热反应来说,反应放热量越大,绝热温升越高,导致后果越严重。
2、绝热温升绝热温升指放热反应物完全转化时所放出的热量可以使物料升高的温度。
3、绝热温升指放热反应物完全转化时所放出的热量可以使物料升高的温度。
4、绝热温升 adiabatic temperature rise 混凝土浇筑体处于绝热状态,内部某一时刻温升值。
5、目前,关于面板坝混凝土面板的温度场及温度应力的研究,主要认为混凝土绝热温升是时间的函数,并未考虑温度对面板水化反应速率及其物理性能的影响。
6、取决于反应的焓变,如是放热反应,随着反应的进行,容器中温度升高,反应速率加快,化学平衡向吸热方向移动。如是吸热反应,容器中温度降低,反应速率减慢,化学平衡向放热方向移动。
解释绝热增温&降温
1、(因热力学第一定律) (4) 相反,当一气团自高空下沉,周围的气压渐渐较该气团为大,因此,气团压缩,内能加大,增温;此即绝热增温。 (5) 焚风的形成: (a) 山背风面的气压低。
2、如果一个受到增温作用或降温作用的系统通过辐射和传导与周围发生热量交换,那么就称之为非绝热过程。【绝热压缩】绝热压缩与绝热膨胀通常由气体压强的变化引起。绝热压缩发生在气压上升时,这时气体温度也会上升。
3、气流下沉所谓的绝热增温效应在理论上是不能成立的:(1)假如一团气流下沉,当它在下降途中由于绝热收缩温度高于周围气温时、那么它必然是受热膨胀、中断下沉、重新上升。
绝热和等温有什么区别?
1、绝热膨胀是指与外界没有热量交换,但等温可逆膨胀跟外界是有联系的,可以进行热量交换。绝热可逆膨胀这个过程中气体体积增大,压强降低,因而温度降低。但等温可逆膨胀就是温度是不会发生变化。
2、等温过程和绝热过程的区别的区别如下:等温过程是过程中温度保持不变,可能有吸热或放热。绝热过程是过程中没有吸放热,但温度可能变化。
3、温度环境不一样 等温可逆膨胀指的在反应过程中温度是恒定不变的,而绝热可逆膨胀指的是内部反应与外界没有热量交换。气体做功不同 绝热可逆膨胀:气体对外界做功,气体膨胀。
4、等温过程可能吸热(一定对外做功),也可能是放热(外界对系统做功)绝热过程和外界没有热交换,外界对系统做功时,温度升高,系统对外界做功时,温度降低。总之这类问题要用热力学第一定律考虑就简单了。
5、绝热膨胀与等温膨胀有什么区别\x0d\x0a在等温过程中,最大限度的热量被转移到了外界,使得系统温度恒定如常。\x0d\x0a绝热过程中,热量没有逃逸,因而温度有上升(下降)。
理想气体在准静态的绝热过程中温度是否发生变化?为什么?
绝热意味着与外界没有热交换,那么压缩时对气体所做的功必然以气体内能的方式进入气体,所以气体内能增加,温度上升。如果你曾经给自行车打过气,你该知道,气筒在打气时会发热。就是这个道理。
【答案】:绝热过程中,由于不吸收热量,系统对外作功是以自身内能减少为代价的,故内能减少,而理想气体的内能是温度的单值函数,所以系统的温度下降。
气体绝热节流,可以肯定的是:焓值不变,压力下降,熵增大。绝热节流前后工质的温度会发生变化,即节流的温度效应,温度可以升高、可以降低、也可以不变(对于理想气体前后温度肯定是不变)。
理想气体的绝热过程,就是,不能和外界有热交换,Q=0, 根据热力学第一定律:△u=Q+w,可得:△u=w 体积变小,也就是w0,内能增加,温度升高,压强增大。
理想气体的绝热指数随温度变化,随着温度的升高而降低,随压力的增加而增加。
虽然理想气体绝热自由膨胀后温度恢复,但整个过程并不是恒温过程。理想气体绝热自由膨胀过程是非准静态过程,除初,末态外,系统每一时刻都处于非平衡态。对于实际气体,温度一般不会恢复到原来温度。
到此,以上就是小编对于绝热过程温度变化怎么计算的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏