本篇目录:
- 1、镁带燃烧的现象
- 2、镁条燃烧化学方程式
- 3、镁带燃烧实验步骤
- 4、镁带燃烧是化学变化吗
镁带燃烧的现象
镁带燃烧的现象:银白色固体在空气中剧烈燃烧,发出耀眼的白光,放出大量热,生成一种粉末状的白色固体物质。镁带燃烧的实验步骤:先用砂纸打磨镁带,然后点燃酒精灯,再用绀埚钳夹持镁带放在酒精灯上加热,观察镁带燃烧。
镁带在空气中燃烧产生的现象如下:镁带空气中燃烧,会发出耀眼的白光。放出大量的热,并伴有白烟产生,生成白色固体。镁条在空气中燃烧时,会发出耀眼的白光,在燃烧的过程中会产生烟雾,并且还会形成一节一节的白色固体。
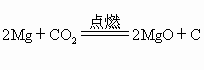
镁条在空气中燃烧:发出耀眼强光,放出大量的热,生成白烟同时生成一种白色物质。镁带介绍:一般指制备成带状的金属镁,化学符号为Mg,外观为有金属光泽的银白色固体。
镁带在氧气中燃烧是一种非常壮观的现象。在没有点燃之前,镁带呈银白色,有金属光泽,但并不显眼。当点燃之后,镁带开始燃烧,发出了耀眼的白光,并且释放出大量的热。
镁条燃烧化学方程式
化学方程式是:2Mg+O2=点燃=2MgO、3Mg+2N2=点燃=2Mg3N2。发生化合反应,镁条剧烈燃烧,发出耀眼的白光,放热,燃烧后有白色粉末生成。
镁条燃烧化学方程式为以下两个 主要反应:2Mg+O2==点燃==2MgO 次要反应:2Mg+CO2==点燃==2MgO+C;3Mg+N2==点燃==Mg3N2 镁条燃烧的文字表达式为:镁+氧气—(点燃)—氧化镁。

盐酸(HCl)和大理石(主要成分是CaCO3)反应,生成氯化钙(CaCl2)、二氧化碳和水,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑。使用 实验时不可用手触摸镁带(有高温)。
镁带燃烧实验步骤
1、上课时镁带刚取出时是黑色的,用砂纸打磨后,去除其氧化膜,是银白色的2用坩埚钳夹持镁带,在酒精灯上点燃,桌面上垫上石棉网,防止燃烧后生成物溅落下来烫坏桌面。
2、取一根镁条,用砂纸反复打磨,以去除镁条表面覆盖的氧化层。打磨前镁条为灰黑色,打磨后呈银白色并带有金属光泽。用老虎钳夹住镁条的一端,用防风打火机从另一端的末梢点燃镁条,加热时使用橘红色的外焰加热。
3、镁带燃烧的实验步骤:先用砂纸打磨镁带,然后点燃酒精灯,再用绀埚钳夹持镁带放在酒精灯上加热,观察镁带燃烧。在这个反应中,镁元素从游离态转变成化合态。物质的颜色由银白色转变成白色。镁可做照明弹。

镁带燃烧是化学变化吗
镁条燃烧是化学变化,现象是生成白色固体,这说明生成了不同于银白色镁条的新物质,符合化学变化的本质特征。
发光的变化不一定是化学变化,例如电灯通电时发光,但是不是化学变化,所以镁条燃烧发出耀眼的白光,不能证明发生了化学变化,生成新物质才是化学变化的本质特征,判断的依据。
有化学变化,没物理变化。物理变化是指物体的状态发生了变化,而化学变化是组成物体的化学键发生了断裂有重新组合生成新的物质。镁带燃烧只是化学变化,生成氧化镁。
镁带空气中燃烧,会发出耀眼的白光。放出大量的热,并伴有白烟产生,生成白色固体。镁条在空气中燃烧时,会发出耀眼的白光,在燃烧的过程中会产生烟雾,并且还会形成一节一节的白色固体。
有现象不一定就发生化学反应,像氢氧化钠溶解在水中会放热,人能感觉到,但却没有发生化学反应。所以化学反应和现象并没有太大关系。镁条在二氧化碳中燃烧是现象,而生成单质碳和氧化镁才是化学变化。
镁条燃烧,从单质镁变成氧化镁,发生了物质改变,这就是化学变化,一种物质变成另一种或多种物质 镁条燃烧时发出眩目的白光,产生热量,这是能看到和感受到的现象。光和热变化属于物理变化。
到此,以上就是小编对于镁带燃烧化学反应的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏