本篇目录:
- 1、物理化学--熵变的计算
- 2、两种不同的气体在等温条件下相互混合熵怎么变化(要求解释)
- 3、相同气体混合熵等为什么为零
- 4、两种气体混合的过程熵变会减小吗?
- 5、25度,将11.2升的氧气和11.2升的氮气混合成11.2升的混合气体,熵变大于...
物理化学--熵变的计算
化学变化用摩尔反应熵算 总熵变=环境熵变+系统熵变 若反应物和产物都处于标准状态下,则反应过程的熵变,即为该反应的标准熵变。
对于一个可逆过程,熵变可以通过热力学第一定律计算:ΔS = Qrev / T 其中,ΔS表示系统的熵变,Qrev表示可逆过程中传递给系统的热量,T表示系统的温度。

ΔS = ∫(dq/T)其中,ΔS是熵变,dq是在过程中吸收的微小热量,T是温度。此公式适用于可逆过程,即系统的状态变化可以逆转而不产生熵的增加。需要注意的是,每种情况下的熵变计算公式都有特定的前提条件和适用范围。
熵变△s计算公式:△S=△H/T。简述 对于化学反应而言,若反应物和产物都处于标准状态下,则反应过程的熵变,即为该反应的标准熵变。当反应进度为单位反应进度时,反应的标准熵变为该反应的标准摩尔熵变。
环境熵变的计算公式:熵变 对于化学反应而言,若反应物和产物都处于标准状态下,则反应过程的熵变,即为该反应的标准熵变。当反应进度为单位反应进度时,反应的标准熵变为该反应的标准摩尔熵变,以△rSm表示。
两种不同的气体在等温条件下相互混合熵怎么变化(要求解释)
因为是等温等压,气体分子间距相等,混乱度一样,所以熵不变。熵,代表混乱度。
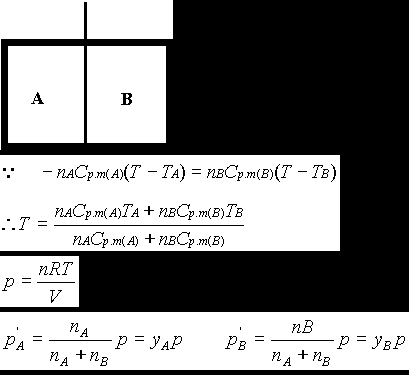
理想气体分子只有动能没有势能,等温过程T不变,分子动能不变,等容过程外界不做功,所以分子内能不变:dQ=0,熵变△S=dQ/T=0。
分子运动范围减小,无序度降低,熵减小。定体降温时,随温度降低,分子运动剧烈程度降低,熵减小。气体等温液化,分子在液体里比气体里运动受限,熵减小。而液体等温气化熵增大。两种气体等温混和使系统无序度增大,熵增大。
熵变(ΔS)是指系统在发生某个过程中的熵的变化。在不同情况下,计算熵变的公式略有不同。
特别是,化学反应中的混合,常常是等温等压条件下的混合,即混合前后子体系与总体系的温度和压强均不发生变化,这种情况下求混合熵就更简单。

相同气体混合熵等为什么为零
1、从统计上来说显然熵变不为零,因为量子态发生改变,即混乱度增加。理论上也有解释,S2-S1=vR*ln2 ,v为总摩尔数,R为普适气体常量。
2、不可逆过程中热量交换会引起熵的增加,因此熵的改变为正值,即△S0。但是由于能量转换是有损耗的,不可逆过程中内能的改变为0,即△U=0。
3、因为熵是状态函数,所以体系熵变为零,其次,因为循环是不可逆的,所以系统加环境的总熵一定大于零,即环境的熵变大于零。对于一个可逆的循环过程,可以分解为很多的微小的循环的积分,在这些微小的循环中熵变为0。
两种气体混合的过程熵变会减小吗?
1、两种气体等温混和使系统无序度增大,熵增大。
2、变大。熵是混乱度的意思,熵越大的物质越稳定,所以化学反应等一般朝着熵变大的方向进行,气体混合也可以同样理解。
3、熵变小于零,吉布斯自由能变大于零。可设为两个过程,先是12升的氧气和12升的氮气等温混合成24升,然后等温压缩为12升。
4、熵会大于零。因为气体熵大于液体熵,液体熵大于固体熵,所以作为气体都是2摩尔但后者的分子量一定大于前者气体的分子量,所以这个反应是一个熵增加的反应,反应后熵一定会大于零。
25度,将11.2升的氧气和11.2升的氮气混合成11.2升的混合气体,熵变大于...
1、摩尔标准状况下,无论是纯的氧气或者是氮气或者是它们任意比得混合气体,1摩尔气体大约占22。另外氧气(O2)和氮气(N2)均是双原子单质,所以12L任意比例的混合气体大约为0.4L体积。
2、从方程式可以看出,H2完全反应,O2有剩余。
3、.5摩尔水,因为有一摩尔氢原子,剩下的气体都是氧气还有0.25摩尔(6L标况),标准状况水全成液体了。
到此,以上就是小编对于混合熵怎么求的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏