本篇目录:
Nacl除杂(MgCl,CaCl,Na2So4)
1、通常用BaCl2除去SO42-,Na2CO3除去Ca2+,NaOH除去Mg2+。
2、用足量的NaCO溶液除去CaCl,用足量的NaOH溶液,除去MgCl,用足量的BaCl溶液,除去NaSO。
3、Na2SO4 + BaCl2 =BaSO4↓ + 2NaCl (2)加入过量的氢氧化钠溶液,除去Mg2+,反应的化学方程式为:MgCl2 +2NaOH=Cu(OH)2↓+2NaCl (3)加入过量的碳酸钠溶液,除去Ca2+和过量的Ba2+,过滤除去沉淀。
4、加NaOH溶液,除去MgCl2。MgCl2+2NaOH=Mg(OH)2↓+2NaCl 加BaCl2溶液,除去Na2SO4。BaCl2+Na2SO4=BaSO4↓+2NaCl 加Na2CO3溶液,除去CaCl2和过量的BaCl2。
nacl除杂naso4.mgcl2.cacl2.有哪些方法过程
用足量的NaCO溶液除去CaCl,用足量的NaOH溶液,除去MgCl,用足量的BaCl溶液,除去NaSO。
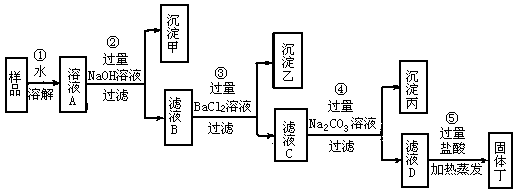
nacl里有(na2co3,na2so4)溶于水,先加过量氯化钡,除去碳酸根离子和硫酸根离子。再加过量碳酸钠,除去多余的钡离子。过滤,再加过量的稀盐酸,蒸发即得纯净的氯化钠。
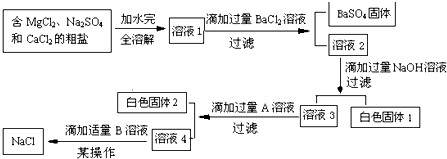
溶解,加过量氢氧化钠与碳酸钠,过滤沉淀,再加过量稀盐酸,最后蒸发结晶。
nahco3 + ca(oh)2 == caco3(沉淀)+na2co3 + 2h2o na2co3+cacl2 == caco3(沉淀)+2nacl nahco3+cacl2 不会反应,因为ca(hco3)2是可溶性的盐,所以没有沉淀、气体以及弱电解质生成,该反应不会发生。
除了最后的盐酸是适量,其他的试剂都是过量。
氯化钠中有二氧化锰怎么除杂?
1、D。氯化钾中含有少量杂质二氧化锰,MnO2是不溶物,而KCl是易溶于水的,通过溶解过滤的物理分离办法即可,不需要化学反应 C。
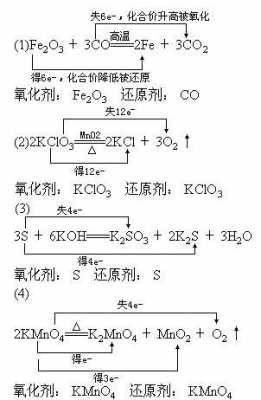
2、初中常用化学除杂方法有以下几种:沉淀法 使混合物中的杂质与适当试剂反应,生成沉淀通过过滤而除去。气体法 将混合物中的杂质与适当试剂反应变成气体而除去。
3、可以用溶解,过滤的方法。原理:二氧化锰是不溶于水的黑色固体,氯化钾是易溶于水物质,故加足量的水溶解后,氯化钾溶于水,二氧化锰沉淀在底部,过滤得到滤渣,洗涤干燥即得到二氧化锰。
如何除去粗盐中的可溶性杂质
1、化学方法去除可溶性杂质 可通过加入溶液,生成沉淀而除去,也可加入 固体和NaOH溶液来除去。(1)在天平上称量剩下的粗盐,计算在10毫升水中大约溶解了多少克粗盐。
2、粗盐中含有泥沙等不溶性杂质,以及可溶性杂质如:Ca2+,Mg2+,SO42- 等。
3、除去粗盐中的可溶性杂质的方法:用盐溶液使杂质离子沉淀,加入试剂顺序:足量的氯化钡溶液,足量氢氧化钠溶液,足量碳酸钠溶液,过滤,然后向滤液中加入适量稀盐酸。
4、粗盐中的杂质主要是CaCl2,MgCl2,和少量硫酸盐 一加氯化钡,形成硫酸钡沉淀,去除硫酸盐,钡离子过量。BaCl2+Na2SO4===BaSO4沉淀+2NaCl 加氢氧化钠,形成氢氧化镁沉淀,氢氧化钙微溶,去除氯化镁。
到此,以上就是小编对于nacl除杂hcl的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏