本篇目录:
怎么判断物质溶解时是放热还是吸热?
1、判断放热反应:全部的燃烧反应(如碳、甲烷燃烧);大部分的化合反应(如氧化钙与水的反应,但只是大部分,也有特吸热例。
2、这两个过程对不同的溶质来说,吸收的热量和放出的热量并不相等,当吸热多于放热,例如硝酸钾溶解在水里的时候,因为它和水分子结合的不稳定,吸收的热量比放出的热量多,就表现为吸热,在溶解时,溶液的温度就降低。

3、物质溶于水一般会有热量的变化,即吸热或放热。一般用温度来衡量。若溶解时放热则温度升高;若吸热则温度降低;若温度无变化则说明物质溶解时既不放热也不吸热。温度的变化在初中阶段一般使用温度计。
4、熔解(化)与凝固的条件 熔化:达到熔点,继续吸热。(非晶体没有熔点)凝固:达到凝固点,继续放热。(非晶体无凝固点)晶体与非晶体的熔解 晶体与非晶体熔解时的性状不同。
5、怎么判断吸热和放热如下:放热反应是放出热量,是释放热量的过程,即周围气体的温度会随之升高,该物体(放热的物体)有可能升温。代表反应类型有:燃烧(氧化)、中和。放热反应的方程式:ΔH0。
6、一是扩散,属于物理变化,吸热;二是水合,属于化学变化,放热。两个过程热效应的多少决定了总体上是吸热还是放热。酸碱溶于水一般放热,典型的是浓硫酸和氢氧化钠。硝酸铵溶于水吸热。记住这三个例子基本就够用了。
蔗糖溶于水的微观解释
1、蔗糖放入水中溶解的微观解释:水分子不断运动。水分子的介绍:水(化学式为H2O),是由氢、氧两种元素组成的无机物,无毒,可饮用。
2、B、间隔不变不可能容纳蔗糖分子,B错C、太离谱,水分解了就不是水了,发生化学反应了,但是蔗糖溶解是物理过程。
3、物理变化。蔗糖溶于水,形成溶液,并没有化学反应发生,只是状态发生改变。物理变化,指物质的状态虽然发生了变化,但一般说来物质本身的组成成分却没有改变。
4、蔗糖晶体在水分子不断撞击下,蔗糖分子离开晶体表面,均匀分散到水中,形成蔗糖溶液。食盐晶体在水分子不断撞击下,钠离子和氯离子离开晶体表面,被水分子包围形成水合钠离子和水合氯离子,均匀分散到水中,形成氯化钠溶液。
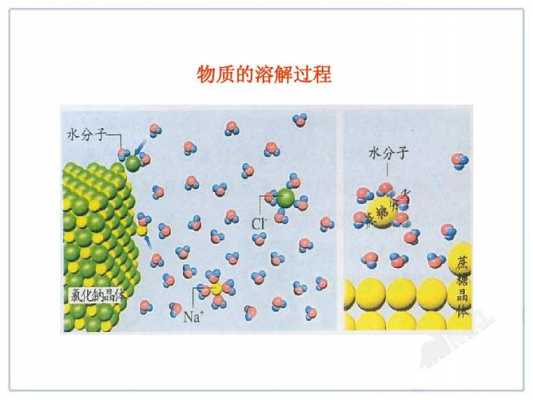
5、因为当蔗糖进入水中时,是蔗糖表面的分子先与水分子接触,并在水分子的作用下向水中扩散,只要没达到饱合,就源源不断的作用,直到达到饱合或蔗糖完全溶解。
溶于水是怎么回事
能够溶解的固体物质在水中溶解的快慢与物体颗粒大小、水的温度 、 液体是否被搅动等因素有关。 固体溶质进入溶液后,首先发生微粒(分子或离子)的扩散(吸热)过程,接着是形成水合离子或水合分子的水合过程(放热)。
简单说,一种物质溶于水就是构成该种物质的分子(离子,原子)在水分子的作用下,彼此分散并被水分子包围,形成水合分子(离子,原子)而稳定地分散在水中形成溶液的过程。
对于有机物来说,小分子有机物溶于水是因为水分子比较大,间隙也大,小分子可以分散到水分子中间,形成水与有机物互溶的现象。比如,水和酒精就是互溶的。
由于气体溶解时体积变化很大,故其溶解度随压强增大而显著增大。水中的二氧化碳会影响水的pH值,如果含有大量二氧化碳会使得水成酸性,因为二氧化碳溶于水生成碳酸。 二氧化碳是空气中常见的温室气体。
物质溶解于水,通常经过两个过程:一种是溶质分子(或离子)的扩散过程,这种过程为物理过程,需要吸收热量;另一种是溶质分子(或离子)和水分子作用,形成水合分子(或水合离子)的过程,这种过程是化学过程,放出热量。
氨气易溶于水,是因为氨气是极性分子,水也是极性分子,而且氨气分子跟水分子还能形成氢键,发生显著的水合作用,所以,它的溶解度很大;而氢气、氮气是非极性分子,所以在水里的溶解度很小。
到此,以上就是小编对于高中化学微溶于水的物质的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏