本篇目录:
- 1、气体的等温变化
- 2、求大佬帮忙看下这道热学题目
- 3、为什么等温条件下气体摩尔体积在减小但是蒸气压却不改变啊,不是有PVm...
- 4、一定质量理想气体,温度不变,体积减小,内能如何变化?
- 5、一定质量气体的,等温变化时,体积减小,分子密集度___,压强增大;等容变化...
气体的等温变化
等温变化:与外界有热交换。理想气体膨胀对外界做功,导热良好,温度不变,是一等温变化,这一过程中,温度不变,即理想气体的内能变化量为0。根据能量守恒定律,气体对外做功,内能不变,则必定吸收外界热量。
由此可见,进入B中的气体原来在A内占的体积为VA-Vx=(10-4)L=6L。
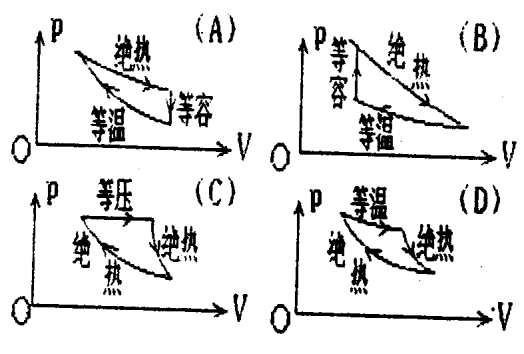
是的,对于理想气体的等温变化有U=0,H=0。
求大佬帮忙看下这道热学题目
1、(2) 在气体缓慢地被活塞压缩回原来的体积的过程中,可以看作是一个等温过程,因为温度保持不变。在等温过程中,外界对气体做的功可以通过理想气体的状态方程计算。初始状态下,气体体积为3V,压强为P/3。
2、根据理想气体状态方程,PV=nRT,可以求出氮气的物态参数。其中,n为摩尔数,R为气体常数,T为气体的绝对温度。
3、v_rms = (3kT/m)^0.5 根据题意,需要计算速率与均方根速率之差不超过均方根速率的1%的分子占总分子数的百分之几。
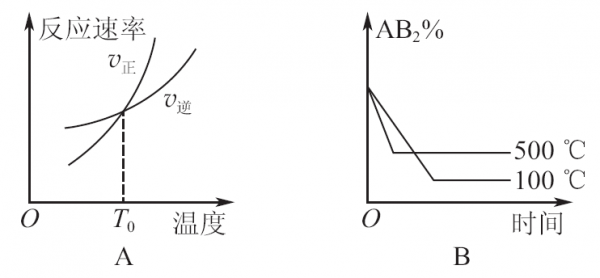
4、水在升高相同的温度时,其吸的热量是相等的。△t温度变化越大,比热容C越小。所以,乙的比热容大 答案为B 谢谢!问题补充:可以理解为,在水中煮的目的是为了使两个金属球的温度最终达到同一个温度。
为什么等温条件下气体摩尔体积在减小但是蒸气压却不改变啊,不是有PVm...
(1)容器是密闭的,所以其体积不变,而Vm=V/n,V和n都不变,所以Vm不变。
偏摩尔体积就是一定量溶质溶在一摩尔溶液中所引起的体积变化,是溶液浓度函数。当溶质为溶液本身即纯溶液时摩尔体积与偏摩尔体积相等。摩尔体积=V÷n,V为物质体积(单位:L);n为物质的量(单位:mol)。
(1)用双手捂住锥形瓶,看看在广口瓶导管口是否有气泡产生,松开手后是否有倒吸的水柱,如果有上述现象出现,说明气密性良好。(3)结果偏小,因为表面的氧化膜包裹了一些Mg,使得一部分没有参加反应。
首先你需要更正一个观念,同温同压的任何气体摩尔体积相等,这句话是没错;但是在同一个容器内,各种不同的气体虽然同温,但是并不同压。
不能,因为标准状态下的水蒸汽压达不到一个标准大气压。说可以的人是在混淆概念。标准状态下任何液体都会有蒸汽,只是很小。
一定质量理想气体,温度不变,体积减小,内能如何变化?
对于理想气体来说,它的内能只与温度有关,只要温度不变,那么它的内能U就保持不变。根据热力学第一定律ΔU=Q+W,也就是理想气体内能的变化量等于吸放热量与做功量的和。
温度没有改变,体积减小 ,压强就增大。如果是外界做功的话内能就是增大。但是如果是在体积减小的情况下有向外放热的话应该是减少。
一定质量的理想气体,等温压缩,即体积变小,所以外力对气体做功。又因为等温变化,气体的温度不变,即内能不变,所以向外释放热量。
温度升高,理想气体的内能增大,温度降低,理想气体的内能减小,温度升高,理想气体的内能增大,理想气体的内能在温度不变时也不变。根据PV=nRT来判断各状态量的变化进而判断温度的变化。
一定质量气体的,等温变化时,体积减小,分子密集度___,压强增大;等容变化...
在这种情况下,体积减小时,分子的密集程度增大,气体的压强就增大。温度、质量一定气体,体积越小,压强越大;体积越大,压强越小。体积、质量一定的气体,温度越小,压强越小;温度越高,压强越大。
Charless Law(查理定律):在恒定压强下,气体的体积与其温度成正比关系。即,当温度升高时,气体的体积也会增加;当温度下降时,气体的体积也会减小。
气体的压强、体积和温度的关系:质量一定的气体在三个参量都变化时所遵守的规律为:PV/T=C(恒量)。P为气体压强 V为气体体积 T为气体温度。
当气体减少时,压强会降低。这是因为减少气体的体积或物质量将减少压强。此外,通过增大容器的体积或降低温度也可以降低气体的压强。需要注意的是,这些因素之间的关系是相互影响的,同时变化也可能会导致不同的结果。
减少,直到等于外界压强就可以平衡。反之气体体积就减小。等容变化;加热气体,气体温度升高,则内能增大,即内部分子的 加剧,对容器[容积不变]壁碰撞就剧烈,压强增大。反之压强减小。
根据PV=nRT,克拉柏龙方程,质量一定,也就是物质的量n一定,R是常数,如果温度不变,体积减小时压强会增大,气体分子的平均动能的量度看温度,此题温度可能不变,不一定非得增大,所以A不对。
到此,以上就是小编对于等温过程体积增大的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏