本篇目录:
- 1、根据热力学第一定律,对微小的状态变化过程有dQ=dW+dE,试对等压、等体...
- 2、等温压缩系数公式
- 3、要用等温压缩的方法使气体液化,需要满足什么条件?
- 4、等温压缩和绝热压缩有什么区别?
- 5、给轮胎打气,怎么实现绝热压缩和等温压缩?
根据热力学第一定律,对微小的状态变化过程有dQ=dW+dE,试对等压、等体...
1、绝热的平衡过程进行中功和能的转换可根据热力学第一定律(dQ=dE+pdV)和绝热过程的特征方程(dQ=0)得到。即dE+pdV=0,从式中看出,在绝热过程中只有系统内能变化时才能做功。
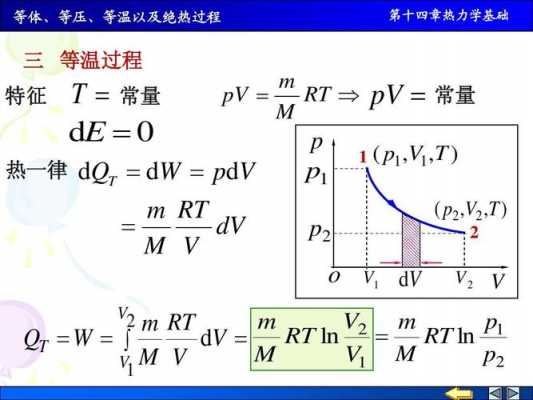
2、热力学第一定律:dU=dq+dw,w为外力对系统做功。∵w=-∫fdl=-∫pSdl=-∫pdV。∴dU=dq-pdV。∵q是关于T的函数,所以U可表示为T、V的函数。
3、内能公式:i是自由度,单原子分子是 3,双原子分子是5;三原子及多原子分子6;n气体的物质的量;R是理想气体常数 R=31J/K。
4、热力学第一定律就是能量守恒定律。不同形式的能量在传递与转换过程中守恒的定律,表达式为△U=Q+W。
5、热力学第一定律是指不同形式的能量在传递与转换过程中守恒的定律,表达式为△U=Q+W。
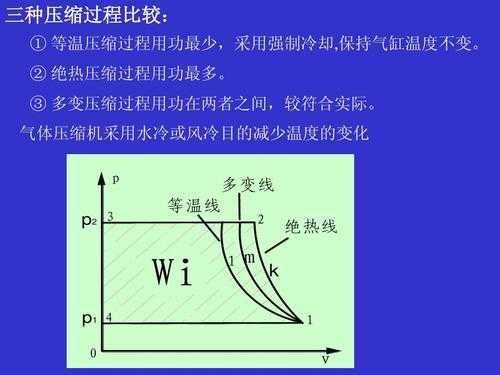
等温压缩系数公式
水在特定温度和压力下的平均压缩系数可以通过公式计算得出:\[ \beta = -\frac{1}{V} \left(\frac{\partial V}{\partial P}\right)_T \]其中,β 是平均压缩系数,V 是体积,P 是压力,T 是温度。
利用公式:Cp-CV=TVα2/β求解。体积膨胀系数(又名体胀系数)是指当物体温度改变1摄氏度时,其体积的变化和它在0℃时体积之比,常用符号α表示。
式中:βf———液体压缩系数,Pa-1,是指在温度不变的条件下,单位体积液体随压力的变化率。
压缩系数公式是z=AP2+BP+C,压缩曲线反映了土受压后的压缩特性,它的形状与土试样的成分、结构、状态以及受力历史有关,压缩性不同的土,其中,e-p曲线的形状是不一样的。
一般取值0.0485。压缩系数的倒数称为体积弹性系数(k),液体的种类不同,其压缩系数和体积弹性系数值也不同。同一种液体的压缩系数和体积弹性系数也随温度和压强而变化,但变化不大,一般可看作为常数。
要用等温压缩的方法使气体液化,需要满足什么条件?
液化是物质从(固态)变成(液态)的过程,需要温度降低到凝固点。实现液化有两种手段,一是降低温度,二是压缩体积。临界温度是气体能液化的最高温度。
使气体液化的两种方法,可以降低温度,或者压缩体积来达到气体液化的目的。一般气体在温度足够低的时候,都可以产生液化。
临界温度高于或接近于室温的气体,如乙醚、氯、氨和某些碳氢化合物,在常温下压缩就可使之液化。临界温度很低的气体,如氧、氮等,须先冷却到临界温度以下,再用等温压缩的方法使其液化。
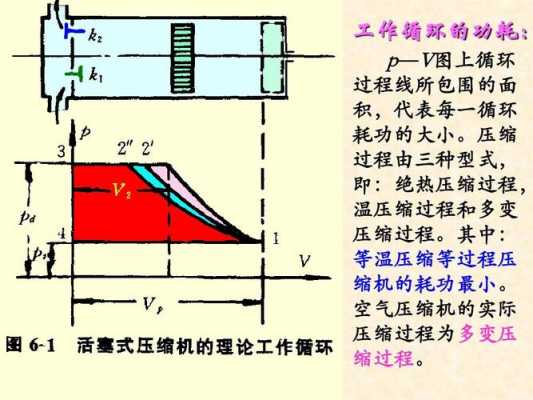
等温压缩和绝热压缩有什么区别?
从字面上讲,前者是在恒温的条件下进行的,后者是在一个绝热的条件下进行的。在等温可逆膨胀过程中系统对环境做的功比绝热可逆膨胀做的功大。
同一状态下等温压缩系数个绝热压缩系数哪一个更大?答案如下:等温压缩系数大,我们要对生活充满希望,一直变好的路上。
等温过程和绝热过程的区别的区别如下:等温过程是过程中温度保持不变,可能有吸热或放热。绝热过程是过程中没有吸放热,但温度可能变化。
温度环境不一样 等温可逆膨胀指的在反应过程中温度是恒定不变的,而绝热可逆膨胀指的是内部反应与外界没有热量交换。气体做功不同 绝热可逆膨胀:气体对外界做功,气体膨胀。
给轮胎打气,怎么实现绝热压缩和等温压缩?
气体迅速被放出,由于这个过程很迅速,来不急和周围环境交换热量,可以近似看成绝热过程,热量等于功加内能,绝热过程热量不变,迅速膨胀对外做功正增大,要保证等式不变,所以内能减小,温度也就降下来了。。
我们有两种压缩氮气的方式:绝热压缩和等温压缩。我们要找出在这两种压缩方式下,氮气体积的变化。假设初始时氮气的温度为 T1 = 300K,压强为 P1 = 10^5Pa,体积为 V1。
绝热压缩发生在气压上升时,气体温度也会上升。例如给自行车打气时,可以感觉到气筒温度上升,这正是因为气体压强上升的足够快到可视为绝热过程的缘故,热量没有逃逸,因而温度上升。
将充气机平放在地面上,显示屏上将显示“0.0”。如果“0.0”显示不正确,请按住中间黄色键5秒钟以上以重置。拧下轮胎气门嘴盖,将其放置到位,然后通过连接器将充气机的充气管拧到轮胎气门嘴上。
到此,以上就是小编对于等温压缩过程如何实现平衡的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏