本篇目录:
溶解和电离一样吗?如果不一样那有什么区别?
1、两者有着根本的不同,溶解是物质之间相互掺杂的过程;而电离是特指电解质在水溶液状态下分解为离子的过程。举个简单的离子,蔗糖溶于水,但是不会发生电离;而NaCl溶于水同时发生电离。
2、实质是很不相同的。当然,万物皆有联系。溶解跟电离自然也有联系。溶解是一群分子均匀分布到另一群分子的过程。它类似于将物质混合均匀。不过是在分子层次上的。
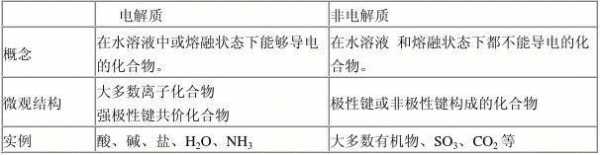
3、水分子不过是帮凶或者载体而已,也就是说“其中的溶解平衡和电离过程是在水分子帮助下实现的”。氯化银固体,有离子,但不能自由移动。有了水的帮助,这些离子才有可能自由移动。
4、电离:有的物质溶解在水中不是以分子的形式存在的而是以离子的形式存在的如硫酸的水溶液中存在的不是硫酸分子,而是氢离子和硫酸根离子;【溶解】 一种物质(溶质)分散于另一种物质(溶剂)中成为溶液的过程。
溶解与电离的区别
电离:有的物质溶解在水中不是以分子的形式存在的而是以离子的形式存在的如硫酸的水溶液中存在的不是硫酸分子,而是氢离子和硫酸根离子;【溶解】 一种物质(溶质)分散于另一种物质(溶剂)中成为溶液的过程。
电离,就是指电解质(分子:如乙酸(醋酸)CH3COOH(C2H4O2)、一水合氨(氨水)NH3·H2O、氢硫酸(硫化氢)H2S、氢氯酸(盐酸 氯化氢)HCl等或晶体,如NaCl、NH4NO3等)在水溶液中或熔融状态下产生自由移动离子的一种过程。
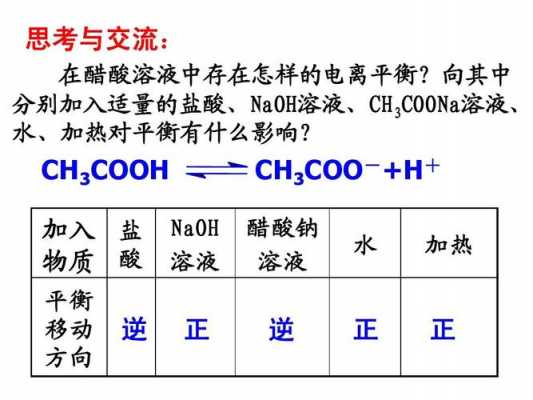
溶解是一群分子均匀分布到另一群分子的过程。它类似于将物质混合均匀。不过是在分子层次上的。但这另一群分子能够接纳多少这种分子,显然是有限度的,而且对于不同的分子,也是有区别的,我们用溶解度来衡量。
氯化银的溶解平衡是可逆的,溶于水的部分是完全电离的,理解成这两个过程的合并才对。然后再去理解教材的解读,会有所帮助。水分子不过是帮凶或者载体而已,也就是说“其中的溶解平衡和电离过程是在水分子帮助下实现的”。
请详解:电解、电离、溶解、分解的区别,万分感谢!
1、电解是在通电的情况下,在阴阳两极发生氧化还原反应。电离是在水溶液或受热融化状态下,电解质产生自由移动离子的过程。
2、电解:使电流通过电解质溶液或熔融电解质而在阴、阳两极引起氧化还原反应的过程。如2NaCl(熔融)=2Na+Cl2 2NaCl+2H2O=2NaOH+H2+Cl2 电离:高中阶段指电解质在水溶液或熔融状态下离解成自由移动的阴阳离子的过程。

3、电解是在电场作用下,造成离子泳动,水解是物质和水发生反应生成其他物质,电离是离子化合物在水中或者在熔融状态下,化合物中两种离子的分离。
4、电解:通电使分解,如:电解水.2H2O==2H2(气)+O2(气)电离:有些物质在水中不是以分子的形式存在的,而是以离子的方式存在的,比如NaCl=Na+ +Cl-这个过程就是电离 水与另一物质分子化合成为一个分子的反应过程。
5、解离,离解和电离三个概念不一样。解离:解离是指化合物或分子在溶剂中释放出离子的过程。解离的程度可以用解离度K来表示。通常来说,解离是吸热反应。
6、电离 就是就是指电解质 在水溶液中或熔融状态下产生自由移动离子的一种过程。溶解 就是溶质 溶于溶剂啊 就像是 食盐溶于水 T T。。
化学电离,水解,溶解
1、都是化学变化。水解是弱离子与水电离出的H+或OH-结合生成弱电解质的过程。电离是生成阳离子和阴离子的过程。溶解平衡乍看起来是溶解(物理变化),但实际是离子与分子的转变(Ag+ + Cl- -- AgCl),仍然是化学变化。
2、电离是在水溶液或受热融化状态下,电解质产生自由移动离子的过程。水解是在水溶液中,盐的离子与水电离出来的H+ 或OH-生成弱电解质的反应,或者是酯、卤代烃等在一定条件下与水反应。
3、沉淀的溶解:(1)生成弱电解质。如生成弱酸、弱碱、水或微溶气体使沉淀溶解。(2)发生氧化还原反应,即利用发生氧化还原反应降低电解质离子浓度的方法使沉淀溶解。
4、溶解平衡和电离平衡有相通的地方,因为大部分物质在水中以离子和少量化合物存在。(强电解质溶液中的化合物可忽略)。所以物质溶解的实质是化合物在水中的电离。
5、首先,水解是指物质与水反应,产生新的化学物质。水解反应通常发生在离子化合物或者某些化学物质与水接触时。而电离是指物质分解成带电离子的过程,其中的分子或者离子与水分子发生相互作用,导致物质分解成带电离子。
沉淀溶解平衡中溶解和电离的区别?
1、可见溶解平衡不局限于弱电解质,强电解质、非电解质只要在水中有溶解度,就存在溶解平衡。电离平衡一定是弱电解质才存在,弱酸、弱碱在水中部分电离,存在电离平衡。
2、根据定义区分:溶解平衡是指分子由晶体进入溶液的速率和由溶液结晶的速率相等;电离平衡是指电离和结合形成分子的速率相等。
3、溶解和电离不一样,溶解是溶质可以分散在溶剂中形成稳定均一的液体,电离一般是溶质中的原子的离子化过程。通常电解质会发生电离,比如白糖溶解在水中就不是电离,但食盐在水中会电离。
4、而电离则是电解质中的阴阳离子被分开了,变成自由移动的阴离子和阳离子。这就类似于将一个分子给拆开了。因此,溶解是分子的分布问题,电离是“分子”的拆开问题。这显然是不种不同的过程。显然实际是不同的。
5、比如硫酸钡溶解度小,但溶解的部分完全电离,硫酸钡是强电解质,不存在电离平衡,写电离方程式是用=表示。
6、电离,就是指电解质(分子:如乙酸(醋酸)CH3COOH(C2H4O2)、一水合氨(氨水)NH3·H2O、氢硫酸(硫化氢)H2S、氢氯酸(盐酸 氯化氢)HCl等或晶体,如NaCl、NH4NO3等)在水溶液中或熔融状态下产生自由移动离子的一种过程。
到此,以上就是小编对于溶解和电离先后顺序的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏