本篇目录:
关于绝热状态方程的问题..
求绝热可逆过程方程的基本思想是利用热力学的第一定律,即能量守恒定律:在没有受到外界力的作用下,在任意绝热可逆过程中,系统的总能量(包括热能和动能)是不变的。
过程见图片:PV=m/M*R*T 理想气体状态方程。这是最基本的方程。绝热过程的方程推导,推荐给你。
(3)实际气体节流膨胀:△H=0,产生致冷或致热效应pv变化,由定义△U不等于零 (4)绝热可逆过程△S=0。可逆过程系统能回到起点而不引起其他变化,实际气体绝热可逆的方程还没有总结出来。
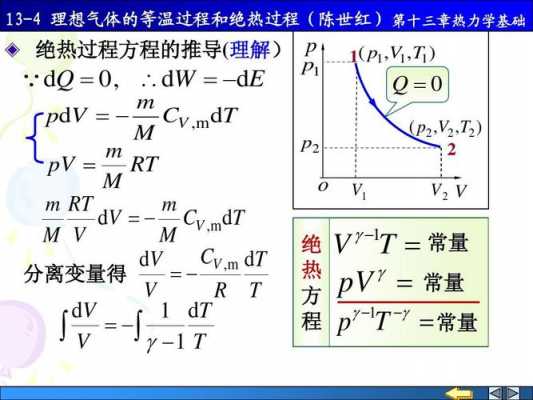
绝热过程方程
关于理想气体,有可逆绝热过程方程,在满足理想气体、绝热、可逆这三个基本条件,才能使用该方程。
绝热可逆过程:Q=0,△U=W=-P外dV(恒外压);或△U=nCv,mdT;△H=nCp,mdT。物体的温度 等温可逆膨胀:物体的温度是恒定的,所以要吸收或者放热的,如果没有外接做功的话同样不能可逆。
方程绝热可逆过程:Q=0,△U=W=-P外dV(恒外压);或△U=nCv,mdT;△H=nCp,mdT。定义 绝热可逆:关于理想气体,有可逆绝热过程方程,在满足理想气体、绝热、可逆这三个基本条件,才能使用该方程。

定压过程:过程进行中系统的压力保持不变;过程方程式:P=常数。
绝热过程的公式是什么?
PdV+VdP=nRdT、dQ=dU+dW=0、pV^(Cp/Cv)=const。绝热过程是一个绝热体系的变化过程,绝热体系为和外界没有热量和粒子交换,但有其他形式的能量交换的体系,属于封闭体系的一种。绝热过程有绝热压缩和绝热膨胀两种。
绝热过程是一个绝热体系的变化过程,其三个公式是指E=NCvT、dW+dE=0、dT=[pdV+Vdp]/NR,即体系与环境之间无热量交换的过程。
W=-p外 (V2-V1),这个式子无论是否可逆都可以使用。系统整个过程中的中间状态不一定都是平衡态,系统的压强可以时时不同(没有一个确定的p),但W=-积分号(p外dV)=-p外积分号(dV)=-p外(V2-V1)。
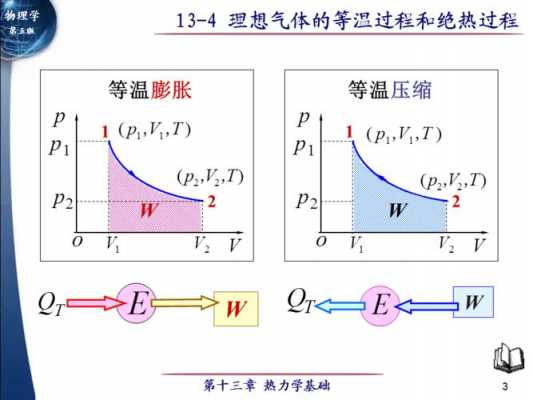
公式如下图:关于理想气体,有可逆绝热过程方程,在满足理想气体、绝热、可逆这三个基本条件,才能使用该方程。
绝热过程表达式: pv^k=C p:压力 v:容积 k绝热指数,对于空气为k=4根据绝热过程的变化规律,由压容图,经积分求得。
理想气体定律、热力学第一定律的内容是什么?
1、理想气体定律:pV=nRT,以下V为摩尔体积,也就是V/n。热容之间关系:Cp=Cv+R,γ(比热比容)=Cp/Cv。热力学第一定律:dU=dq+dw,w为外力对系统做功。∵w=-∫fdl=-∫pSdl=-∫pdV。∴dU=dq-pdV。
2、热力学第一定律 内容:物体内能的增量(ΔU)等于外界对物体做的功(W)和物体吸收的热量(Q)的总和。表达式:W+Q=ΔU。
3、热力学第一定律数学表达式 △U=Q+W。△U内能的该变量 Q热量 W表示功。外界对系统做功,w为正值;系统对外界做功,w为负值。
4、(1)理想气体,恒温过程:△U,△H=0。不可逆过程:△S大于零 ;△A,△G小于零 (2)理想气体节流膨胀过程:△H=0,温度不变于是△U=0。
到此,以上就是小编对于气体绝热变化的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏