本篇目录:
- 1、如何制造硫酸?
- 2、浓硫酸是如何制备?
- 3、求浓硫酸制取方法?
- 4、硫酸怎么制作出来的
- 5、硫酸的工业制备过程有哪些?
- 6、工业制硫酸化学方程式制备流程是怎样的
如何制造硫酸?
1、制取二氧化硫(沸腾炉),然后在接触室接触氧化为三氧化硫,再用浓度为93%的硫酸吸收三氧化硫得到焦硫酸,焦硫酸加水得到硫酸。最后提纯。
2、硫酸的制备方法如下:先将硫黄或黄铁矿在空气中燃烧或焙烧,以得到二氧化硫气体。 将二氧化硫氧化为三氧化硫是生产硫酸的关键,其反应为:2SO2+O2→2SO3。

3、二水法磷酸反应后,利用磷石膏,工业循环利用,使用二水法制硫酸。方法二 制取二氧化硫(沸腾炉)2 4FeS2+11O2=高温=8SO2+2Fe2O3 将二氧化硫溶于水变成亚硫酸。亚硫酸氧化得硫酸。
4、工业制法 生产硫酸的原料有硫黄、硫铁矿、有色金属冶炼烟气、石膏、硫化氢、二氧化硫和废硫酸等。硫黄、硫铁矿和冶炼烟气是三种主要原料。
5、实验室制法 可以用FeSO7H2O加强热,用冰水混合物+U型管冷凝即可,用NaOH吸收SO2,理论可得25%的H2SO4。关键在于尾气吸收。 可将二氧化硫气体通入双氧水制取硫酸,此法占率较低。
浓硫酸是如何制备?
工业上制造硫酸有两种方法:一种叫做接触法,一种叫做铅室法。铅室法的硫酸浓度低而且往往含有很多杂质,用途受到限制,已逐步被淘汰,目前应用最多的为接触法。

硫酸的制备方法如下:先将硫黄或黄铁矿在空气中燃烧或焙烧,以得到二氧化硫气体。 将二氧化硫氧化为三氧化硫是生产硫酸的关键,其反应为:2SO2+O2→2SO3。
黄铁矿制取二氧化硫。将二氧化硫氧化成三氧化硫。用93%硫酸吸收三氧化硫。将工业浓硫酸进行蒸馏,便可得到浓度95%-98%的商品浓硫酸。
先把需要的水量好( 1000-107=893 mD,再把浓硫酸量好,把浓硫酸沿着杯壁缓缓加入到水中,并不断的搅拌。
其他方法:磷酸反应后,利用磷石膏,工业循环利用,使用二水法制硫酸。较为经典的制法还有利用草酸和硫酸亚铁反应。

求浓硫酸制取方法?
1、工业上制造硫酸有两种方法:一种叫做接触法,一种叫做铅室法。铅室法的硫酸浓度低而且往往含有很多杂质,用途受到限制,已逐步被淘汰,目前应用最多的为接触法。
2、硫酸的生成可以通过多种方法进行,其中最常见的方法是通过硫磺的氧化反应得到。
3、可将工业浓硫酸进行蒸馏,便可得到浓度95%-98%的商品硫酸。二水法磷酸反应后,利用磷石膏,工业循环利用,使用二水法制硫酸。
4、其他方法:磷酸反应后,利用磷石膏,工业循环利用,使用二水法制硫酸。较为经典的制法还有利用草酸和硫酸亚铁反应。
硫酸怎么制作出来的
首先,在氧气存在的条件下,硫元素(S)可以发生氧化反应,变为二氧化硫(SO2)。S + O2 → SO2 接下来,二氧化硫会与水(H2O)反应,形成硫酸并释放大量的热量。这个反应被称为硫酸的水合反应。
先将硫黄或黄铁矿在空气中燃烧或焙烧,以得到二氧化硫气体。 将二氧化硫氧化为三氧化硫是生产硫酸的关键,其反应为:2SO2+O2→2SO3。 根据二氧化硫转化成三氧化硫途径的不同,制造硫酸的方法可分为接触法和硝化法。
硫酸的生成可以通过多种方法进行,其中最常见的方法是通过硫磺的氧化反应得到。
在亚硝酸中加入过氧化氢,使其氧化然后得到硫酸。
准备原料:需要准备硫矿石(一种含有较高含量的硫的矿石),空气和水。炼制硫酸气体:首先将硫矿石粉碎并加入高温炉中,加入足够的空气使其氧化。这个过程将产生二氧化硫(SO2)气体。将二氧化硫通过冷凝过程冷却并收集。
工业制法:制取二氧化硫(沸腾炉)4FeS2+11O2=高温=8SO2+2Fe2O3 将二氧化硫溶于水变成亚硫酸。亚硫酸氧化得硫酸。硫酸是一种最活泼的二元无机强酸,能和许多金属发生反应。
硫酸的工业制备过程有哪些?
1、制取二氧化硫(沸腾炉),然后在接触室接触氧化为三氧化硫,再用浓度为93%的硫酸吸收三氧化硫得到焦硫酸,焦硫酸加水得到硫酸。最后提纯。
2、工业制硫酸化学方程式:H2S2O7+H2O═2H2SO4。制备流程:(1)制取二氧化硫(沸腾炉):燃烧硫或高温处理黄铁矿,制取二氧化硫。
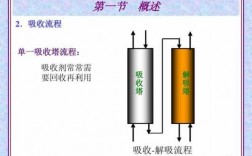
3、接触法生产工艺:接触法的基本原理是应用固体催化剂,以空气中的氧直接氧化二氧化硫。其生产过程通常分为二氧化硫的制备、二氧化硫的转化和三氧化硫的吸收三部分。
4、主要方程式:4FeS2+11O2=2Fe2O3+8SO2 2SO2+O2=2SO3 SO3+H2O=H2SO4 硫酸(化学式:H 2SO 4), 硫的最重要的 含氧酸。
5、二水法磷酸反应后,利用磷石膏,工业循环利用,使用二水法制硫酸。
6、问题一:工业如何制硫酸 接触法制硫酸的原理、过程及典型设备 1.三种原料:硫铁矿(FeS2)、空气、水。利用接触法制硫酸一般可以用硫黄、黄铁矿、石膏、有色金属冶炼厂的烟气(含一定量的SO2)等。
工业制硫酸化学方程式制备流程是怎样的
制取二氧化硫(沸腾炉),然后在接触室接触氧化为三氧化硫,再用浓度为93%的硫酸吸收三氧化硫得到焦硫酸,焦硫酸加水得到硫酸。最后提纯。
工业上制取盐酸时,首先在反应器中将氢气点燃,然后通入氯气进行反应,制得氯化氢气体。氯化氢气体冷却后被水吸收成为盐酸。
FeS2+11O2=2Fe2O3+4SO2 S+O2=SO2 (两者条件都是点燃)第二步,纯化二氧化硫,除去由于燃烧而产生的烟尘,特别是冶金废气,和黄铁矿燃烧产生的SO2。第三步,干燥SO2,为SO2的转换作准备,常用的是浓硫酸。
用五氧化二钒做催化剂该反应为可逆反应)用93%硫酸吸收SO3+H2SO4═H2S2O7(焦硫酸),加水(吸收它)H2S2O7+H2O═2H2SO4提纯工艺,可将工业浓硫酸进行蒸馏,便可得到浓度95%-98%的商品硫酸。
工业制硫酸:4FeS2+11O2=8SO2+2Fe2O3,2SO2+O2=2SO3,SO3+H2O=H2SO4。工业制取硝酸:4NH3+5O2=4NO+6H2O,2NO+O2=2NO2,3NO2+H2O=2HNO3+NO。
到此,以上就是小编对于浓硫酸是什么变化的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏