本篇目录:
- 1、为什么理想气体的自由膨胀过程是绝热过程?
- 2、理想气体自由膨胀是什么过程?
- 3、理想气体的自由膨胀是怎样的过程
- 4、真空自由膨胀、绝热自由膨胀、等温自由膨胀的特点
- 5、等温膨胀过程到底是怎样的一个过程?
- 6、理想气体等温膨胀的规律。
为什么理想气体的自由膨胀过程是绝热过程?
绝热过程。自由膨胀过程 由于体系经历绝热过程,故与外界无热交换。又由于气体向真空自由膨胀,外压为零,故体系对环境做功也为零。
由于体系经历绝热过程,故与外界无热交换。又由于气体向真空自由膨胀,外压为零,故体系对环境做功也为零。
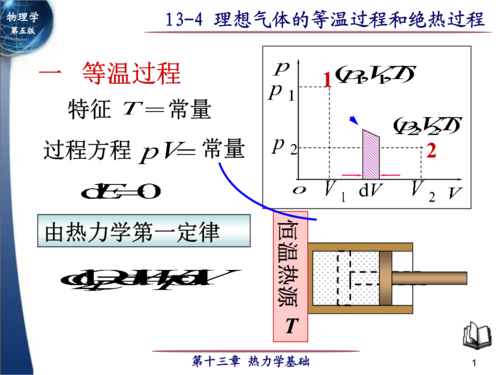
Q=W功+W内。理想气体在真空环境下的膨胀不对外做任何功,即W功为零,理想气体可以忽略分子间作用力,即W内可以视为零。所以吸热量Q为零,即绝热状态。
自由膨胀过程 由于体系经历绝热过程,故与外界无热交换。又由于气体向真空自由膨胀,外压为零,故体系对环境做功也为零。
理想气体自由膨胀是什么过程?
在一个刚体绝热系统中理想气体进行自由膨胀的过程为不可逆过程,在该过程中,压力和温度会发生变化,故其为多变过程。
绝热过程。自由膨胀过程 由于体系经历绝热过程,故与外界无热交换。又由于气体向真空自由膨胀,外压为零,故体系对环境做功也为零。
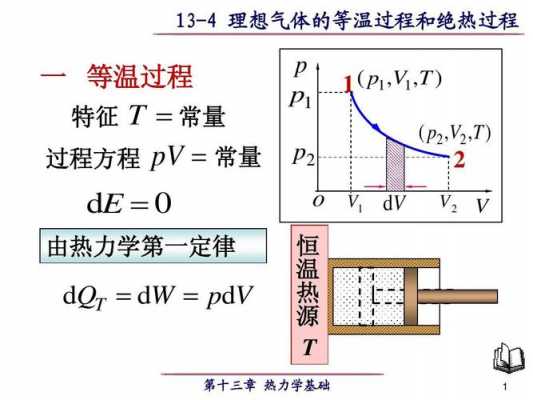
理想气体的自由膨胀:A、是绝热过程;B、也是等温过程。真实气体的自由膨胀:A、是绝热过程;B、但不是等温过程。
理想气体真空自由膨胀是不可逆过程,如何计算这一过程的熵变呢?理想气体向真空自由膨胀,由于初、终两态温度不变(设为T),只是体积由V1增大到V2,所以可用理想气体等温膨胀的可逆过程来连接初、终两态。
由于体系经历绝热过程,故与外界无热交换。又由于气体向真空自由膨胀,外压为零,故体系对环境做功也为零。
自由膨胀过程表示不对外做功。热力学第一定律:如果气体的内能不变,那么就不对外放热也不从外界吸热。所以你的前提是理想气体内能不变。
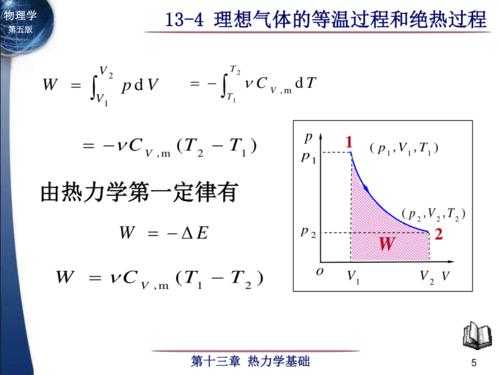
理想气体的自由膨胀是怎样的过程
绝热过程。自由膨胀过程 由于体系经历绝热过程,故与外界无热交换。又由于气体向真空自由膨胀,外压为零,故体系对环境做功也为零。
在一个刚体绝热系统中理想气体进行自由膨胀的过程为不可逆过程,在该过程中,压力和温度会发生变化,故其为多变过程。
自由膨胀:气体在膨胀时只有受到外界的阻碍作用,如有活塞密闭、活塞外有气体等情况,即所谓有“外界”的存在,才会对外做功,而一旦所谓的“外界”没有的话,如活塞无质量,活塞另一侧是真空等情况,气体膨胀时就不对外做功。
理想气体真空自由膨胀是不可逆过程,如何计算这一过程的熵变呢?理想气体向真空自由膨胀,由于初、终两态温度不变(设为T),只是体积由V1增大到V2,所以可用理想气体等温膨胀的可逆过程来连接初、终两态。
真空自由膨胀、绝热自由膨胀、等温自由膨胀的特点
特征:理想气体与外界没有热量交换。2规律:准静态绝热膨胀过程中理想气体的压强跟体积满足绝热方程:V=常数。
理想气体的真空自由膨胀的过程是一种不可逆的热力学过程,理想气体过程中气体在一个绝热的系统膨胀,外界和系统之间没有功和热的交换。理想气体向真空膨胀,温度不发生变化,真实气体向真空膨胀,温度一定降低。
自由膨胀:气体在膨胀时只有受到外界的阻碍作用,如有活塞密闭、活塞外有气体等情况,即所谓有“外界”的存在,才会对外做功,而一旦所谓的“外界”没有的话,如活塞无质量,活塞另一侧是真空等情况,气体膨胀时就不对外做功。
膨胀效应:由于真空环境中热量传递的困难性,物体在真空中的温度升高更为迅速,导致膨胀效应更为明显。另外,自由膨胀和真空膨胀的膨胀系数也有所不同,因为在真空中物体的膨胀受到的限制更小,所以真空膨胀系数通常较大。
等温膨胀过程到底是怎样的一个过程?
等温过程是热力学过程的一种,即是指热力学系统在恒定温度下发生的各种物理或化学过程。在整个等温过程中,热量的传递使系统与其外界处于热平衡状态。
温度不变,压力减小。 比如一个针筒,在封闭了的情况下,拉开,这就是一个膨胀过程,如果温度不变,那么就是一个等温膨胀的过程。
等温膨胀:所谓等温膨胀就是指一定质量的理想气体在温度不变的条件下缓慢进行的膨胀过程.可见等温膨胀是准静态过程。特征:温度不变,体积增大。
理想气体等温膨胀的规律。
1、所谓等温膨胀就是指一定质量的理想气体在温度不变的条件下缓慢进行的膨胀过程.可见等温膨胀是准静态过程。特征:温度不变,体积增大。
2、气体等温膨胀△S的变化:理想气体向真空膨胀,温度不发生变化,真实气体向真空膨胀,温度一定降低。理想气体经过恒容无非体积功的过程,有ΔH=nCp,mΔT。(假设Cp,m是常数)。
3、所以等温膨胀时,由于温度不变,因此焓和内能也不变,即焓变和内能变化均为零.理想气体分子只有动能没有势能,等温过程T不变,分子动能不变,等容过程外界不做功,所以分子内能不变:dQ=0,熵变△S=dQ/T=0。
4、根据热力学第一定律ΔU=Q+W,也就是理想气体内能的变化量等于吸放热量与做功量的和。 Q指的是气体吸放热情况,气体吸热,Q取正值;气体放热,Q取负值。
5、一次膨胀,压强骤减,只有一段,分步有n段,分步至无限次就是的积分。对于理想气体,等温可逆过程△U=△H=0。W=-nRTlnV2/V1,Q=-W。绝热可逆过程:Q=0,△U=W=-P外dV(恒外压)。或△U=nCv,mdT,△H=nCp,mdT。
6、绝热自由膨胀过程中,压强、体积两个量的变化关系的确与等温膨胀中这两个量的变化关系相同,即p2v2=p1v1。定压热容与定体热容的比值称为摩尔热容比,用符号γ表示,大小等于(i+2)/i,其中i是理想气体的自由度。
到此,以上就是小编对于等温自由膨胀用什么判据的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏