本篇目录:
- 1、NaCl溶解后就变成了纳离子和氯离子了?
- 2、氯化钠的电解方程式是什么?
- 3、氯化钠电解方程式
- 4、NaCl水中溶解电离
- 5、NaCl和HCl在水中电离的电离过程有什么不同
- 6、nacl电离方程式
NaCl溶解后就变成了纳离子和氯离子了?
氯化钠nacl属于强电解质,溶解在水中后,全部电离成钠离子(na+)和氯离子(cl-)。当水少了,浓度增大,氯化钠又会逐渐的形成晶体小颗粒,这是由于溶解平衡造成的,当水干了后,又会变回小晶体。
是的,氯化钠(NaCl)溶于水后会建立电离平衡。当氯化钠溶于水时,晶格中的NaCl分子会解离成离子形式,即钠离子(Na^+)和氯离子(Cl^-)。

因为氯化钠是离子晶体,由钠离子和氯离子以离子键的形式构成。溶于水时,离子键受破坏,所以在溶液中产生的是游离的氯离子和钠离子。
在一般情况下,氯化钠固体不能导电,但是氯化钠溶解在水中,就形成了氯化钠溶液。由于氯化钠溶于水后电离成了阴离子氯离子和阳离子钠离子,这些离子在水中可以自由移动,因此氯化钠溶液可以导电。
氯化钠的电解方程式是什么?
1、氯化钠电解方程式是:2NaCl+2H2O=点解=Cl2↑+H2↑+2NaOH。离子方程式为2Cl-+2H2O=通电=H2↑+Cl2↑+2OH-。
2、电解氯化钠(溶液)反应方程式:2NaCl+2H2O==电解==2NaOH+2H2↑+2Cl2↑(氯碱工业的反应)。阴极反应:2Cl-(氯离子)- 2e = Cl2↑(氯气),阳极反应:2H+ + 2e = H↑。
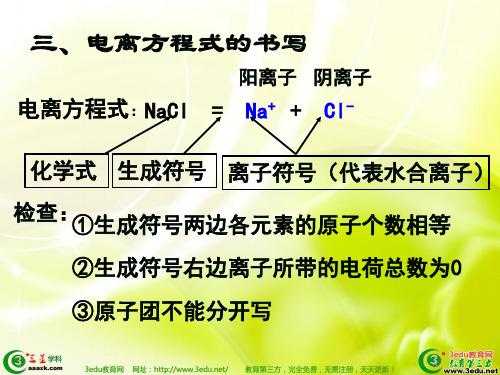
3、电解氯化钠方程式:2NaCl(熔融)==电解==2Na+ Cl↑ H在阴极上不断得到电子而生成氢气放出,破坏了附近的水的电离平衡,因而水分子大量电离成H和OH。且生成OH的快慢远大于其向阳极定向运动的速率。
氯化钠电解方程式
1、氯化钠电解方程式是:2NaCl+2H2O=点解=Cl2↑+H2↑+2NaOH。离子方程式为2Cl-+2H2O=通电=H2↑+Cl2↑+2OH-。
2、电解氯化钠(溶液)反应方程式:2NaCl+2H2O==电解==2NaOH+2H2↑+2Cl2↑(氯碱工业的反应)。阴极反应:2Cl-(氯离子)- 2e = Cl2↑(氯气),阳极反应:2H+ + 2e = H↑。
3、电解氯化钠方程式:2NaCl(熔融)==电解==2Na+ Cl↑ H在阴极上不断得到电子而生成氢气放出,破坏了附近的水的电离平衡,因而水分子大量电离成H和OH。且生成OH的快慢远大于其向阳极定向运动的速率。

4、电解氯化钠溶液的方程式为:2NaCl+2H2O=2NaOH+H2↑+Cl2↑ (反应条件为电解)。阴极反应:2Cl-(氯离子) - 2e = Cl2↑ (氯气)。
NaCl水中溶解电离
是的,氯化钠(NaCl)溶于水后会建立电离平衡。当氯化钠溶于水时,晶格中的NaCl分子会解离成离子形式,即钠离子(Na^+)和氯离子(Cl^-)。
NaCL=NA+ +CL- NaNO3=Na+ +NO3- BaSO4=Ba2+ +SO4 2- 欢迎追问。
氯化钠溶液中水的电离程度10^-7mol/L。
氯化钠溶于水是物理变化。化学变化的概念通俗讲就是生成新物质,从微观角度来说,就是原子重新排列组合成新的分子。
NaCl和HCl在水中电离的电离过程有什么不同
1、电离,就是指电解质分子:如乙酸CH3COOH、一水合氨NH3·H2O、氢硫酸H2S、盐酸HCl等;晶体,如NaCl、NH4NO3等)在水溶液中或熔融状态下产生自由离子的一种过程。
2、电离:高中阶段指电解质在水溶液或熔融状态下离解成自由移动的阴阳离子的过程。这个过程是自发进行的,无需外加电场作用。
3、NaCL的溶解既有水合也有扩散。氯化钠溶于水实际是水分子将氯离子和钠离子从晶体表面拉下来并包围起来,形成水合离子,然后再扩散到水中各处,最后形成均一的、稳定的混合物。扩散是简单的物理过程,而水合是化学变化。
nacl电离方程式
电离方程式:NaCl=Na++Cl-,CH3COONH4=CH3COO-+NH4+。
电解氯化钠(溶液)反应方程式:2NaCl+2H2O==电解==2NaOH+2H2↑+2Cl2↑(氯碱工业的反应)。阴极反应:2Cl-(氯离子)- 2e = Cl2↑(氯气),阳极反应:2H+ + 2e = H↑。
电解氯化钠(熔融状态)方程式:2NaCl(熔融)==电解==2Na+ Cl2↑电解氯化钠(溶液)反应方程式:2NaCl+2H2O==电解==2NaOH+2H2↑+2Cl2↑氯碱工业的反应。
氯化钠电解方程式是:2NaCl+2H2O=点解=Cl2↑+H2↑+2NaOH。离子方程式为2Cl-+2H2O=通电=H2↑+Cl2↑+2OH-。
电解氯化钠反应方程式:2NaCl + 2H2O === 2NaOH + H2↑ + Cl2↑ (反应条件为电解)食盐水中的氯化钠(NaCl)和水(H2O)发生电离,通电后分别在阴极与阳极生成氢气(H2)与氯气(Cl2)。
NaCl的电离方程式 NaCl == Na+ + Cl-,没有水。2 NaCl + 2 H2O ==通电== 2 Na+ + 2 OH- + H2↑ + Cl2 这不是NaCl的电离方程式,这是NaCl溶液电解的方程式。电离是自发的,不需要外加电流。
到此,以上就是小编对于nacl电离方程式怎么写的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏